2 附录XIII A 无特定病原体鸡胚质量检测要求
无特定病原体(SPF)鸡系指在严格控制饲养条件下,符合所规定的微生物学检测要求的鸡。无特定病原体鸡胚是指SPF鸡生产的受精卵,在符合生物制品生产的条件下,经孵化后所生成的鸡胚。通过对SPF鸡蛋和SPF鸡群病原微生物的检测,使SPF鸡胚质量得以控制。
2.1 检测项目与方法
检测要求 | ||
鸡白痢沙门菌Salmonella pullorum | ● | SPA, IA, TA |
● | AGP, HI | |
● | AGP, SN, HI | |
传染性法氏囊病病毒 Infectious Bursal Disease Virus | ● | AGP, SN |
● | AGP, SN | |
新城疫病毒 Newcastle Disease Virus | ● | |
禽痘病毒 Fowl Pox Virus | ● | AGP |
马立克病病毒 Marek's Disease Virus | ● | AGP |
副鸡嗜血杆菌 Haemophilus paragallinarum | ● | SPA |
多杀巴斯德菌 Pasteurella multocida | ○ | AGP |
检测要求 | ||
禽腺病毒Ⅲ群(EDS)Avian Adenovirus Group Ⅲ | ● | |
鸡毒支原体 Mycoplasma gallisePticum | ● | SPA, HI |
滑液囊支原体 Mycoplasma synoviae | ● | SPA, HI |
● | AGP, EST, SN | |
● | ||
● | AGP | |
● | AGP | |
禽腺病毒Ⅰ群 Avian Adenovirus Group I | ● | AGP |
● | IFA |
2.2 【附注】
HI,血凝抑制试验;
ELISA,酶联免疫吸附试验;
EST,胚敏感试验;
SN,血清中和试验;
TA,试管凝集试验;
IFA.间接免疫荧光试验。
2.3 检测要求
(1)取样 禽淋巴白血病病毒和禽脑脊髓炎病毒的检测均应取新鲜鸡蛋。其他病原微生物检测一律检测血清,每份供试品血清量应不少于1ml。必须按无菌操作程序取样,防止污染。
(2)取样数量 淋巴白血病病毒检测,每个鸡群取鸡蛋200枚(少于200只的鸡群从全群中取样),每只鸡取蛋1枚。禽脑脊髓炎病毒检测,每个鸡群取鸡蛋不少于50枚(少于50只鸡的鸡群应从全群中取样),每只鸡取蛋1枚。其他病原微生物感染检测,应采取随机方式取样,抽取每个鸡群的5%,少于200只鸡的鸡群应按10%~15%抽样。
(3)供试品的保存与运输 取样后应尽快将供试品送往检测实验室检验。不能及时运送的供试品,血清须在-15℃以下保存,鸡蛋应在4~10℃保存。保存时间应不超过1周。供试品应有明显的编号标志,并附送检单,写明鸡群名称、鸡群数量、供试品名称及数量。供试品在运送过程中应避免温度上升,防止破损。
2.4 结果判定
3 附录XIII B 实验动物微生物学检测要求
本标准(引自GB 14922.2—2001)适用于豚鼠、地鼠、兔、犬、猴和清洁级及以上小鼠、大鼠。
3.1 1.实验动物微生物学等级分类
(1)普通级动物Conventional (CV) Animal 不携带所规定的人兽共患病病原和动物烈性传染病的病原。
(2)清洁动物Clean.(CL) Animal 除普通动物应排除的病原外,不携带对动物危害大和对科学研究干扰大的病原。
(3)无特定病原体动物Specific Pathogen Free (SPF)Animal 除清洁动物应排除的病原外,不携带主要潜在感染或条件致病和对科学实验干扰大的病原。
(4)无菌动物Germ Free (GF) Animal 无可检出的一切生命体。
3.2 2.检测要求
(1)外观指标 动物应外观健康、无异常。


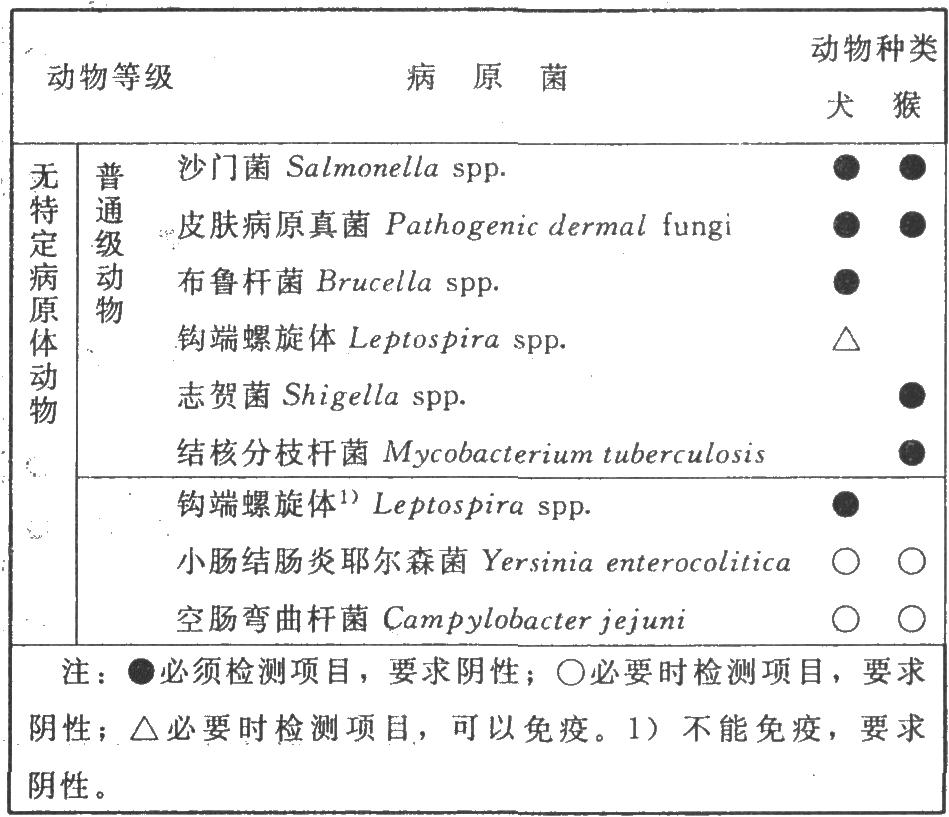



4 附录XIII C 实验动物寄生虫学检测要求
本标准(引自GB 14922.1—2001)适用于地鼠、豚鼠、兔、犬、猴和清洁级及以上小鼠、大鼠。
4.1 1.实验动物寄生虫学等级
(1)普通级动物Conventional (CV) Animal不携带所规定的人兽共患寄生虫。
(2)清洁动物Clean (CL) Animal 除普通动物应排除的寄生虫外,不携带对动物危害大和对科学研究干扰大的寄生虫。
(3)无特定病原体动物Specific Pathogen Free (SPF)Animal除普通动物、清沽动物应排除的寄生虫外,不携带主要潜在感染或条件致病和对科学实验干扰大的寄生虫。
(4)无菌动物Germ Free(GF)Animal 无可检出的一切生命体。
4.2 2.检测要求
(1)外观指标 动物应外观健康,无异常。

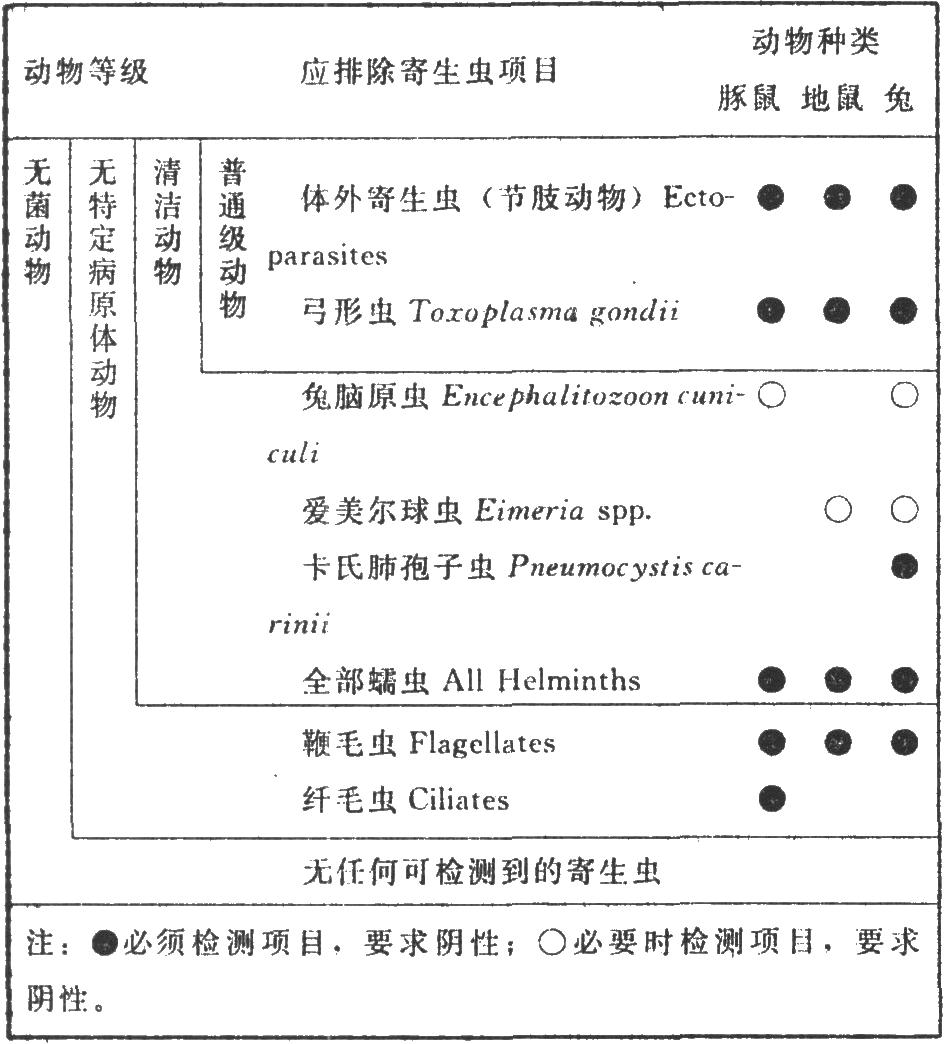

5 附录XIII D 新生牛血清检测要求
本品系从出生14小时内未进食的新生牛采血分离血清,经除菌过滤后制成。牛血清生产过程中不得任意添加其他物质成分。新生牛血清用于生产前应逐批进行以下检查,并应符合规定。
5.1 蛋白质含量
应为3.5%~5.0%(2010年版药典三部附录Ⅵ B 第一法)。
5.2 血红蛋白
用氰化高铁法或其他适宜的方法测定。应不高于0.02%。
5.3 大肠杆菌噬菌体
5.4 渗透压摩尔浓度
应为250~400mOsmol/kg(2010年版药典三部附录V H)。
5.5 无菌检查
依法检查(2010年版药典三部附录Ⅻ A),应符合规定。
5.6 支原体检查
依法检查(2010年版药典三部附录Ⅻ B),应符合规定。细菌内毒素检查 应不高于10EU/ml(2010年版药典三部附录Ⅻ E 凝胶限度试验)。
5.7 病毒检查
5.7.1 1.细胞培养法
(1)非血吸附病毒检查 将新生牛血清供试品分别接种到人源(如人二倍体细胞)、猴源(如Vero细胞)以及牛肾传代细胞3种细胞,采用的牛肾传代细胞系应证明无牛病毒的污染。每种细胞至少接种6瓶,每瓶细胞悬液接种量应不少于培养液总量的25%。置36℃±1℃培养21天。接种的每种细胞都应同时设立牛血清阴性对照和病毒阳性对照(阴性对照用牛血清应证明无牛病毒污染)。培养过程中可根据细胞生长情况更换细胞培养液,每次更换培养液前应观察有无细胞病变出现。培养到期后,阴性对照应无任何细胞病变出现,阳性对照应出现典型的细胞病变,试验成立。供试品检查不出现任何细胞病变为阴性,符合要求。
(2) 血吸附病毒检查 将上述接种供试品的每种细胞取2瓶进行血吸附病毒检查。用0.2%~0.5%鸡和豚鼠红细胞混合悬液覆盖于细胞表面,置2~8℃30分钟,然后置90~25℃作用30分钟,分别进行镜检,观察红细胞吸附情况,供试品检查结果均应为阴性。试验同时应设立血吸附阳性对照。
5.7.2 2.免疫荧光抗体检查法
采用直接或间接免疫荧光抗体检查法,至少应对牛腹泻病毒、牛腺病毒、牛细小病毒、呼肠孤病毒、狂犬病病毒以及牛副流感病毒进行检查,结果均应为阴性。
支持细胞增殖检查 用Sp2/O-Ag14或适宜的非贴壁传代细胞进行。
(1)细胞生长曲线的测定 取供试品按10%浓度配制细胞培养液,按每1ml含104个细胞的细胞浓度接种细胞,每天计数活细胞,连续观察1周,并绘制生长曲线,细胞的最大增殖浓度应不低于每1ml含106个细胞。
(2)细胞倍增时间的测定 按Sp2/O-Ag14细胞生长曲线计算细胞的倍增时间。取细胞峰值前一天的细胞计数(Y)、接种细胞数(X)及生长时间(T)计算。

细胞的倍增时间应不超过20小时。
(3)克隆率的测定 按有限稀释法将细胞稀释,并按每孔1个细胞的浓度接种于96孔细胞培养板,每板至少接种48孔,于37℃、5%二氧化碳条件下培养1周后计算克隆率,应不低于70%。
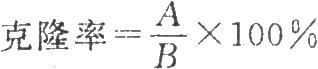
B为接种细胞的总孔数。