1 拼音
W S / T 7 8 1 — 2 0 2 1 biàn xié shì xiě táng yí lín chuáng cāo zuò hé zhì liàng guǎn lǐ zhǐ nán
3 基本信息
ICS 11.020
CCS C 50
中华人民共和国卫生行业标准WS/T 781—2021《便携式血糖仪临床操作和质量管理指南》(Guidelines for clinical operation and quality managementofportable blood glucose meters)由中华人民共和国国家卫生健康委员会于2021年04月19日《关于发布《儿童血细胞分析参考区间》等3项推荐性卫生行业标准的通告》(国卫通〔2021〕3号)发布,自2021年10月01日起实施。
4 发布通知
关于发布《儿童血细胞分析参考区间》等3项推荐性卫生行业标准的通告
国卫通〔2021〕3号
现发布《儿童血细胞分析参考区间》等3项推荐性卫生行业标准,编号和名称如下:
WST 781—2021 便携式血糖仪临床操作和质量管理指南
上述标准自2021年10月1日起施行。
特此通告。
国家卫生健康委
2021年4月19日
5 前言
本文件按照 GB/T 1.1—2020《标准化工作导则 第 1 部分:标准化文件的结构和起草规则》的规定起草。
本文件代替 WS/T 226—2002《便携式血糖仪血液葡萄糖测定指南》。本文件起草单位:复旦大学附属中山医院、国家卫生健康委临床检验中心、浙江大学附属邵逸夫医院、中国医科大学附属第一医院、复旦大学附属华山医院、浙江大学附属第一医院。本文件主要起草人:潘柏申、陈文祥、谢鑫友、郭玮、李小英、王蓓丽、郭晓临、关明、吴建平。
6 标准正文
6.1 1 范围
本文件规定了便携式血糖仪进入医疗机构应用的性能要求和使用其进行血糖监测的质量管理要求。本文件适用于医疗机构使用便携式血糖仪开展血糖监测,不包括患者自我监测。2 规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅所注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GB/T 19634—2005 体外诊断检验系统自测用血糖监测系统通用技术条件3 术语与定义
下列术语和定义也适用于本文件。
3.1
便携式血糖仪 portable blood glucose meters
可随身携带、操作便捷、在患者近旁使用、快速测定患者末梢血中葡萄糖浓度的设备。其给出的葡萄糖测定浓度可以是末梢全血葡萄糖浓度,也可以校准为血浆葡萄糖浓度(目前市场上后者居多)。
3.2
在患者近旁进行的、采用便携式分析仪器并具有操作简便和能快速得到检测结果的检测方式。
3.3
精密度 precision
在规定的条件下,独立检测结果间的一致程度,精密度的度量通常以不精密度表示。[来源:WS/T 407—2012,3.3]
3.4
可比性 comparability
使用不同的测量程序测定某种分析物获得的检测结果间的一致性。结果间的差异不超过规定的可接受标准时,可认为结果具有可比性。
[来源:WS/T 407—2012,3.1]
3.5
测量区间 measuring interval
在规定条件下,由具有一定的仪器不确定度的测量仪器或测量系统能够测量出的一组同类量的量值,又称分析测量范围(analytic measuring range,AMR)。
[来源:WS/T 420—2013,3.3]
3.6
标准差 standard deviation,SD 一个数据集中各数据与平均数离差平方的平均数的平方根,反映数据集的离散程度。
3.7
变异系数 coefficient of variation,CV
3.8
危急值 critical value
某项或某类检测异常结果,当这种检测异常结果出现时,表明患者可能处于有生命危险的边缘状态,临床医生需要及时得到检测信息,迅速给予患者有效的干预措施或治疗,就可能挽救患者生命,否则有可能出现严重后果,失去最佳抢救机会。
6.2 4 缩略语
下列缩略语适用于本文件。
BGMS 血糖监测系统(blood glucose monitoring system)
SMBG 血糖自我监测(self-monitoring blood glucose)
GOD 葡萄糖氧化酶(glucose oxidase)
GDH 葡萄糖脱氢酶(glucose dehydrogenase)
NAD-GDH 烟酰胺腺嘌呤二核苷酸葡萄糖脱氢酶(nicotinamide adenine dinucleotideglucosedehydrogenase)
FAD-GDH 黄素腺嘌呤二核苷酸葡萄糖脱氢酶(flavin adenine dinucleotide glucosedehydrogenase)
PQQ-GDH 吡咯喹啉醌葡萄糖脱氢酶(pyrroloquinoline quinone glucose dehydrogenase)
Mut.Q-GDH 喹啉蛋白葡萄糖脱氢酶突变体(mutant variant of quinoprotein glucosedehydrogenase)
HCT 红细胞压积(hematocrit)
HIS 医院信息系统(hospital information system)
LIS 实验室信息系统(laboratory information system)EQA 室间质量评价(external quality assessment)
PT 能力验证试验(proficiency testing)
6.3 5 便携式血糖仪进入医疗机构应用的性能要求
6.3.1 5.1 总则
新品牌、新型号的便携式血糖仪首次进入医院正式用于临床前,需选取2~3 台仪器、2~3个批号的试纸进行必要的性能验证,确认此款血糖仪是否满足临床需求,是否适用于医院复杂的医疗环境,是否属于 BGMS 而非 SMBG 设备。评价指标至少包括:精密度、与生化分析仪的可比性、测量区间、抗干扰性能。此外,需确认信息化功能是否满足院内患者血糖监测和质量管理的需求。
6.3.2 5.2 精密度
根据 GB/T 19634—2005《体外诊断检验系统自测用血糖监测系统通用技术条件》的要求:当血糖浓度<5.5 mmol/L时,标准差(SD)<0.42 mmol/L;当血糖浓度≥5.5 mmol/L时,变异系数(CV)<7.5%。评价方法详见附录B。
6.3.3 5.3 与生化分析仪的可比性
当血糖浓度<5.5 mmol/L时,至少95%的检测结果差异在±0.83 mmol/L的范围内;当血糖浓度≥5.5mmol/L时,至少95%的检测结果差异在±15%的范围内。评价方法详见附录C。
6.3.4 5.4 测量区间
制造商声明的测量区间至少需覆盖2.2 mmol/L~22.2 mmol/L的范围,有特殊病情监测需要且有条件的医疗机构可选择测量区间更宽的仪器。
6.3.5 5.5 抗干扰性能
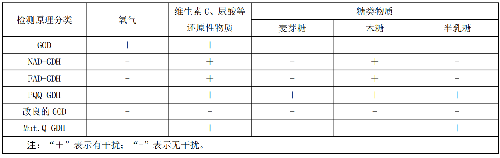
6.3.5.1 5.5.1 类葡萄糖物质
采用GDH法的便携式血糖仪易受麦芽糖、木糖、半乳糖的影响,使检测结果偏高。
6.3.5.2 5.5.2 影响氧化还原反应的因素
a) 还原性物质:维生素 C、对乙酰氨基酚、尿酸等会影响酶的氧化还原反应,使便携式血糖仪检测结果偏高;
6.3.5.3 5.5.3 红细胞压积(HCT)
HCT在35%~55%区间内时,便携式血糖仪通常可正常使用。当超出这个范围时,需注意便携式血糖仪检测数据的准确性。HCT偏高可导致检测结果偏低;HCT偏低可导致检测结果偏高。5.5.4 其他因素
a) 体内代谢物:胆红素、甘油三酯、尿酸、肌酐等达到一定浓度时,会影响便携式血糖仪的检测结果;
b) pH 值、温湿度等因素也会影响便携式血糖仪的检测结果。
临床出现便携式血糖仪检测结果与实验室检测结果偏差较大时,需考虑临床症状以及用药对检测结果产生的可能影响。
6.3.5.4 5.5.5 抗干扰性能验证
WS/T 781—20214影响不同检测方法便携式血糖仪的常见干扰物质见附录D,必要时可进行抗干扰性能验证。可接受的范围为:当血糖浓度<5.5 mmol/L时,干扰物质引起的差异较空白标本不超过0.55 mmol/L;当血糖浓度≥5.5 mmol/L时,干扰物质引起的差异较空白标本不超过10%。
6.3.6 5.6 信息化要求
便携式血糖仪需能与医院信息系统(HIS)以及实验室信息系统(LIS)相连接,或配备专用的管理软件,有助于实现全院室内质控的实时监控、试纸开瓶有效期的监控,满足医疗机构对便携式血糖仪信息化管理的要求。
宜选用具有远程锁定功能的便携式血糖仪,当遇到非资格认证的操作人员、试纸超过有效期、质控失控等影响检测结果准确性的情况时由管理人员锁定,待存在问题纠正后方可重新用于检测。
6.4 6 院内血糖监测质量管理建议
6.4.1 6.1 成立院内 POCT 管理机构
POCT管理机构可由相关科室组成,宜包括医务管理部门(牵头)、检验科、护理部及内分泌科等,下设相关小组分管不同工作。宜设专人负责院内POCT管理机构工作。院内POCT管理机构需制定并定期更新POCT仪器清单,每家医疗机构使用的同一功能的POCT仪器品牌不宜过多。
6.4.2 6.2 制定便携式血糖仪血糖监测相关的文件和记录
6.4.2.1 6.2.1 标准化操作规程
以血糖监测系统制造商的介绍为依据制定相关文件,至少包括以下标准化操作规程:
b) 仪器操作标准化操作规程;
d) 结果报告标准化操作规程;
e) 废弃物处理标准化操作规程;
以上文件可根据医院具体情况进行补充或合并。
6.4.2.2 6.2.2 记录
根据标准化操作规程制定相应记录(纸质或电子),至少包括(不限于):a) 检测记录:患者信息、标本检测结果、检测日期与时间、试纸批号及有效期、仪器编号、操作人员等;
b) 质控记录:质控品检测结果、质控日期与时间、试纸批号及有效期、仪器编号、操作人员、失控判断与处理等;
c) 室间质评记录:质评标本检测结果、检测日期与时间、试纸批号及有效期、仪器编号、操作人员、回报结果分析与处理等;
d) 比对记录:比对标本检测结果、比对日期与时间、试纸批号及有效期、仪器编号、操作人员、比对通过标准与判断等;
e) 危急值报告记录;
f) 仪器校准与维护保养记录。
规范保存各类记录,至少2年。
6.4.3 6.3 人员培训、考核与授权
便携式血糖仪的操作培训考核由医院POCT管理机构主持,制造商积极配合。医院POCT管理机构定期组织相关操作人员的培训和考核,记录并保存培训及考核结果。经过培训且考核合格的人员经授权后方能从事临床便携式血糖仪的检测活动。
培训内容至少涵盖以下内容:
c) 标本采集流程;
g) 仪器、试纸及质控品的储存条件;
j) 生物安全预防措施。
6.4.4 6.4 建立便携式血糖仪质量控制体系
6.4.4.1 6.4.1 分析前质量控制
6.4.4.1.1 6.4.1.1 标本采集
根据制造商建议的标本类型制定标本采集的标准化操作规程,末梢血标本采集方案及注意事项见附录A。
6.4.4.1.2 6.4.1.2 仪器维护与校准
按制造商介绍的要求做好维护保养与定期校准(可由制造商工程师执行),使仪器始终处于良好的工作状态,以确保检测结果的准确性。
6.4.4.1.3 6.4.1.3 试纸准备
按制造商介绍的要求储存、使用试纸,暂时不用时迅速盖好瓶盖,以防止试纸变质,新开瓶时需标注开启日期和使用者,在开瓶有效期内使用。
6.4.4.2 6.4.2 分析中质量控制
6.4.2.2 质控频次:每个检测日至少进行 1 次质控,包含高、低 2 个浓度水平。如充分评估过仪器和试剂的稳定性,可在不增加额外风险的前提下,根据评估情况制定质控频次及质控品浓度水平。
6.4.2.3 质控范围与规则:如使用配套质控品,至少使用制造商提供的浓度范围作为质控范围,超出范围判定为失控;如使用第三方质控品,需参考常规定量检测项目建立质控范围,使用13S和22S质控规则。
6.4.2.4 确保仪器处于正常工作状态,做好室内质控、室间质评,一旦出现失控情况,锁定仪器无法进行患者标本检测,进行失控分析和纠正措施,质控在控后方可解锁重新检测患者标本。
6.4.4.3 6.4.3 分析后质量控制
6.4.3.2 结果报告要素至少包括:患者信息、检测人员、检测日期与时间、检测结果。可出具正式报告(需有检验资质)或记录于病程录。
6.4.3.3 当检测结果落在“危急值”范围内时,立即向医生(如检测人员为护士或检验人员)或上级医生(如检测人员为医生)报告并及时处理,同时采集静脉血送检验科生化分析仪复检。“危急值”需根据临床医生建议确定。
6.4.5 6.5 与生化分析仪的比对
医疗机构每年至少进行1次便携式血糖仪与本医疗机构检验科生化分析仪之间的方法学比对,每次5份标本,详细方案及注意事项见附录C。对于比对不通过的仪器,需进行原因分析和整改,改进后再次比对,仍旧无法达到要求的,不宜继续使用。
6.4.6 6.6 室间质量评价(EQA)/能力验证试验(PT)
医疗机构每年至少参加1次国内或国外相关机构举办的EQA/PT活动,参加的医疗单元(便携式血糖仪使用频率高、检测结果对临床决策影响大的医疗单元)宜相对固定,参加的仪器需覆盖全院使用的主要品牌,其余仪器与之进行比对,比对方案可参照生化比对方案。
7 附录A(规范性附录)便携式血糖仪血糖检测标准化操作规范
7.1 A.1 消毒
选用75%乙醇或50%异丙醇消毒采血部位,不可选择对检测结果有干扰的消毒剂(如碘伏)。待消毒剂干燥后进行采血。
7.2 A.2 采血
首选采集指尖(新生儿足跟)末梢血进行检测,避免选择水肿、感染、末梢循环不良的部位。采血针穿刺皮肤后,轻压使血液自然流出,用消毒干棉球轻拭去第1滴血液后,将第2滴血液滴入试纸上的指定区域。
穿刺皮肤后不可过度用力挤压,以免组织液混入血液标本造成检测结果偏差。
7.3 A.3 检测
7.4 A.4 检测结果记录
记录需包括:被测试者(患者)姓名、检测日期与时间、检测结果与单位、检测者签名等。A.5 异常结果处理
出现血糖异常结果时,需分析原因,针对不同的原因采取处理措施,如复测、复测质控后重新检测、重新采集静脉血使用生化分析仪检测、复测后通知临床医生采取必要的干预措施。
8 附录B(规范性附录)便携式血糖仪精密度评价方案
8.1 B.1 验证方法
收集肝素(如制造商有推荐的抗凝剂类型,首选推荐类型)抗凝的静脉血标本(HCT在制造商声明的适宜范围内)至少2份,一份中值或高值标本(≥5.5 mmol/L),一份低值标本(<5.5 mmol/L),每份标本在检测前充分混匀,分别重复检测20次,计算有效检测结果的SD和CV。
8.2 B.2 结果判断
当血糖浓度<5.5 mmol/L时,标准差(SD)<0.42 mmol/L;当血糖浓度≥5.5 mmol/L时,变异系数(CV)<7.5%。
9 附录C(规范性附录)便携式血糖仪与生化分析仪的比对方案
9.1 C.1 标本准备
9.1.1 C.1.1 抗凝剂选择
采用肝素(如制造商有推荐的抗凝剂类型,首选推荐类型)抗凝静脉血标本(HCT在制造商声明的适宜范围内)进行比对试验。每份标本使用全血进行便携式血糖仪检测,离心分离的血浆进行生化分析仪检测。
9.1.2 C.1.2 浓度要求
浓度涵盖:接近4.1.3推荐的测量区间低限(2.2 mmol/L)、参考区间内、医学决定水平(7.0mmol/L、11.0 mmol/L)左右、接近4.1.3推荐的测量区间高限(22.2 mmol/L)。
9.1.3 C.1.3 标本来源
C.1.3.1 未经人为处理的标本
为了更好地验证结果相关性,排除分析前因素的影响,需尽量采用未经人为处理的静脉血标本进行比对。如低值和高值标本确实难以获取,可使用新鲜标本进行制备。
C.1.3.2 低浓度标本制备
可选择血糖浓度为4 mmol/L~5 mmol/L的静脉血标本,将其放在37℃温箱中孵育6 h使葡萄糖酵解,即可获得血糖浓度2.8 mmol/L左右的标本。检测前室温平衡至少15 min。
C.1.3.3 高浓度标本制备
可通过加入一定稀释比例(具体根据原始标本血糖浓度计算)的50%葡萄糖注射液(277.8mmol/L)获得高浓度标本,加入的葡萄糖注射液体积尽量小,使其对标本基质的影响最小。检测前室温平衡至少15 min。
9.1.4 C.1.4 标本预处理
按照便携式血糖仪介绍的要求和方法学原理对标本进行预处理。为避免糖酵解带来的误差,需保证每份标本的便携式血糖仪检测与生化分析仪检测之间的时间间隔不超过30 min。
9.2 C.2 仪器选择
每个医疗单元选取每种品牌、型号各1台便携式血糖仪与生化分析仪进行比对,比对通过后医疗单元内其他便携式血糖仪再与其进行比对,标本要求与制备方法同上。
9.3 C.3 判断标准
9.3.1 C.3.1 便携式血糖分析仪与生化分析仪比对判断标准
当血糖浓度<5.5 mmol/L时,检测结果差异在±0.83 mmol/L的范围内;当血糖浓度≥5.5mmol/L时,检测结果差异在±15%范围内。
对于新仪器初次性能评估,每台便携式血糖仪,检测合格率需达到95%以上才能判断此仪器为可比性合格的仪器。
对于年度比对,每台便携式血糖仪,检测合格率需达到80%以上才能判断此仪器为可比性合格的仪器,即5份标本中有4份标本检测结果达到上述要求。
9.3.2 C.3.2 便携式血糖仪间比对判断标准
11 参考文献
[1] GB/T 19634—2005 体外诊断检验系统自测用血糖监测系统通用技术条件
[2] CNAS-CL38:医学实验室质量和能力认可准则在临床化学检验领域的应用说明
[3] 中华医学会检验医学分会,卫生部临床检验中心,中华检验医学杂志编辑委员会.POCT临床应用建议.中华检验医学杂志,2012,35(1):10-16
[4] 宋蓓,周志男,王丹,等.医院内POCT血糖室间质量评价方法的建立.国际检验医学杂志,2019,40(18):2298-2301
[5] ISO 15197 2013.In vitro diagnostic test systems-Requirements for blood-glucosemonitoring systems for self-monitoring in managing diabetes mellitus
[6] CLSI POCT 07-A Quality Management:Approaches to Reducing Errors at the Point ofCare;Approved Guideline
[7] CLSI POCT 09-A Selection Criteria for Point-of-Care Testing Devices;Approved Guideline
[8] CLSI POCT 12-A3:Point-of-Care Blood Glucose Testing in Acute and ChronicCareFacilities; Approved Guideline—Third Edition
[9] National Academy of Clinical Biochemistry Laboratory Medicine. GuidelinesandRecommendations for Laboratory Analysis in the Diagnosis and Management of Diabetes Mellitus.Washington,DC:American Association for Clinical Chemistry Inc,2011
[10] Burtis CA,Bruns DE. Tietz fundamentals of clinical chemistry.7th ed. St.Louis,Missouri:Elsevier Inc,2015
[11] Tang Z,Du X,Louie RF,et al. Effects of drugs on glucose measurements with handheldglucose meters and a portable glucose analyzer. Am J Clin Pathol,2000,113(1):75-86
[12] Vote DA,Doar O,Moon RE,et al. Blood glucose meter performance under hyperbaricoxygen conditions. Clin Chim Acta,2001,305(1-2):81-87
[13] Ginsberg BH.Factors affecting blood glucose monitoring :sources of errorsinmeasurement. J Diabetes Sci Technol,2009,3(4):903-913
[14] Guzel O,Guner EI.ISO 15189 accreditation:Requirements for quality and competenceof medical laboratories,experience of a laboratory I. Clin Biochem,2009,42(4-5):274-278
[15] American Diabetes Assosiation. Diagnosis and classification of diabetes mellitus.Diabetes Care 2010,33(Suppl 1):S62-S69
[16] Medicines and Healthcare products Regulatory Agency.Blood glucose meters:point-of-care testing. https://www.gov.uk/government/uploads/system/uploads/attachment_data/file/371870/Blood_glucose_meters_-_point-of-care_testing.pdf