3 基本信息
ICS 13.280
C 57
中华人民共和国卫生行业标准 WS 533—2017《临床核医学患者防护要求》(Requirements for patient radiation protection in clinical nuclear medicine)由中华人民共和国国家卫生和计划生育委员会2017年5月18日《关于发布〈职业性放射性肿瘤判断规范〉等9项卫生标准的通告》(国卫通〔2017〕4号)发布,本标准自2017年11月1日起施行。
4 发布通知
国卫通〔2017〕4号
现发布《职业性放射性肿瘤判断规范》等9项卫生标准,其编号和名称如下:
一、强制性国家职业卫生标准:
GBZ 97—2017 职业性放射性肿瘤判断规范(代替GBZ 97—2009);
GBZ 98—2017 放射工作人员健康要求(代替GBZ 98—2002);
GBZ 112—2017 职业性放射性疾病诊断总则(代替GBZ 112—2002);
GBZ 121—2017 后装γ源近距离治疗放射防护要求(代替GBZ 121—2002);
GBZ 131—2017 医用X射线治疗放射防护要求(代替GBZ 131—2002);
GBZ 178—2017 粒籽源永久性植入治疗放射防护要求(代替GBZ 178—2014)。
二、推荐性国家职业卫生标准
三、强制性卫生行业标准
四、推荐性卫生行业标准
WS/T 549—2017 尿中总铀和铀-235/铀-238比值分析方法 电感耦合等离子体质谱法(ICP——MS)
上述标准自2017年11月1日起施行,GBZ 97—2009、GBZ 98—2002、GBZ 112—2002、GBZ 121—2002、GBZ 131—2002、GBZ 178—2014同时废止。
特此通告。
国家卫生计生委
2017年5月18日
5 前 言
本标准第 4 章~第 5 章为强制性的,其余为推荐性的。
本标准按照 GB/T 1.1-2009 给出的规则起草。
本标准由GB 16361-2012《临床核医学的患者防护与质量控制规范》转化而来。与GB 16361-2012相比,主要技术变化如下:
——删除了药物质量控制的一般要求内容及相关内容,保留了放射性药物施用量质量控制要求;
本标准起草单位:中国医学科学院放射医学研究所、中国医学科学院肿瘤医院、中国疾病预防控制中心辐射防护与核安全医学所、四川省疾病预防控制中心 。
本标准主要起草人:张良安、耿建华、张文艺、丁艳秋、焦玲、何玲、杨翊。
本标准所代替标准的历次版本发布情况为:
——GB 16361-1996;
——GB 16361-2012。
6 标准正文
6.1 1 范围
本标准规定了临床核医学正当性判断、放射防护最优化、医疗照射剂量约束和异常医疗照射的调查与处理等方面的患者防护要求。
本标准适用于将放射性核素用于临床核医学的诊断与治疗,不包括放射性粒子源植入的情况。
6.2 2 规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GBZ 120 临床核医学放射卫生防护标准
GBZ 179 医疗照射放射防护基本要求
6.3 3 术语和定义
下列术语和定义适用于本文件。
3.1
放射性药物 radiopharmaceutical
以诊断或治疗人类疾病或生理状况为目的任何含有放射性原子的化学化合物。应用放射性药物时,不仅应像任何其他药物一样考虑其化学和生物学特性,还应考虑其辐射防护和安全问题。
3.2
放射化学纯度 radiochemical purity
在含有以一种特定化学形态存在的某种放射性药物中,以该种特定化学形态存在的放射性核素质量占总放射性核素质量的百分比。
6.4 4 一般要求
6.4.1 4.1 对临床核医学诊断治疗单位的要求
4.1.1 核医学单位应制定全面的质量保证大纲,该大纲至少包括附录 A 中 A.1 建议的内容。
4.1.2 核医学单位应建立健全包括患者防护在内的管理制度和操作流程,该管理制度和操作流程至少包括附录 A 中 A.2 建议的内容。
4.1.3 应配备与其服务项目相适应并且性能合格的核医学诊疗设备(包括相关辅助设备)、放射防护与放射性药物施用量质量控制仪器、个人防护用品。
4.1.4 应按附录 A 的规范,使用活度计对施用的放射性核素活度进行抽样质控检测,抽样测量的准确度应优于 5%;应按国家相关规定定期对活度计进行检定或校准,取得合格和有效的检定或校准证书。
4.1.5 应设置与其服务项目相适应并且符合 GBZ 120 防护要求的各种工作场所及其相应防护设施;加强对注射或口服放射性药物后患者的管理。
4.1.6 应设立放射防护和质量保证管理组织,各类医技人员应在各自的工作中严格遵循防护和安全要求以及质量控制要求,并承担相应的责任。
4.1.7 应针对实施诊疗时可能出现的故障或失误,制定应急预案,并进行应急培训和演练,将可能出现的故障或失误所致后果减到最小。
6.4.2 4.2 对临床核医学执业医师及相关人员的要求
4.2.1 执业医师开具的放射性药物诊疗申请及放射性药物处方应严格掌握适应证,对临床核医学诊疗敏感的患者严格控制这类诊疗。
4.2.2 核医学专业执业医师应逐例对开具的放射性药物诊疗申请及处方进行正当性审核,尤其应注意孕妇和哺乳妇女患者。
4.2.3 在临床核医学诊疗实施前,执业医师、护士及临床核医学技师有责任将可能的风险以口头或书面形式告知患者或其家属。
4.2.4 执业医师及其他相关工作人员,除应具备相应专业技能外,还应接受核医学诊疗的防护知识等技术培训。
6.5 5 正当性判断
6.5.1 5.1 一般要求
5.1.1 所有新型临床核医学诊疗技术和方法,临床核医学部门在使用前都应通过正当性判断;已判断为正当的技术和方法,当取得新的或重要的证据并需要重新判断时,应对其重新进行正当性判断。
5.1.2 临床核医学医师应掌握各种医学影像诊疗技术的特点及其适应证,使用时应严格控制其适应证范围。新技术和方法即使已做过正当性判断,在用于新的适应证前,还应另行进行正当性判断。
5.1.3 执业医师在开具放射性药物诊疗申请及放射性药物处方前,应注意查阅以往患者检查资料,尽量避免不必要的重复检查。
5.1.4 为了避免对胎儿、胚胎和婴儿造成意外辐射照射,应对患者是否怀孕或哺乳进行询问。并将有关咨询说明张贴在临床核医学部门醒目位置处,特别是入口处和候诊区。
5.1.5 除本标准的规定外,还应满足GBZ 179中正当性判断的其他要求。
6.5.2 5.2 诊断中的正当性判断
5.2.1 除有临床指征并必须使用放射性药物诊断技术外,宜尽量避免对怀孕和可能怀孕的妇女使用诊断性放射性药物;若必须使用时,应告知患者胎儿可能存在潜在风险。
5.2.2 除有临床指征并必须使用放射性药物诊断技术外,应尽量避免对哺乳期妇女使用放射性药物;若必须使用时,应建议患者按附录B的建议适当停止哺乳。
5.2.3 除有临床指征并必须使用放射性药物诊断技术外,通常不宜对儿童实施放射性核素显像检查,若需对儿童进行这种检查,应按附录C的建议减少放射性药物施用量,而且应可能选择半衰期短的放射性核素。
6.5.3 5.3 治疗中的正当性判断
5.3.1 除非是挽救生命的情况,对怀孕和可能怀孕的妇女不应实施放射性药物的治疗,特别是含 I-131和 P-32 的放射性药物。为挽救生命而进行放射性药物治疗时,应按附录 D 的方法对胎儿接受剂量进行评估,并告知患者胎儿可能存在潜在风险。
5.3.2 除非是挽救生命的情况外,宜尽量避免对哺乳期妇女进行放射性药物治疗;若必须使用时,应建议患者按附录 B 的建议适当停止哺乳。
6.6 6 放射防护最优化
6.6.1 6.1 一般要求
6.1.1 临床核医学执业医师审查放射性药物诊疗申请及处方时,应采用以下措施,使患者接受的剂量尽可能的低:
a)根据不同患者的身体特点选用适当的放射性药物及其施用活度,特别要注意儿童与器官功能损害的患者;
b)对非检查器官应尽量使用阻断放射性药物吸收的方法,并使其加速排除;
c)注意采用适当的图像采集和处理技术;
d)要充分应用已有的信息,避免一切不必要的重复照射;
e)应参考附录 E 中相应的医疗照射指导水平。
6.1.3 应对已施用放射性药物的患者提供书面和口头的指导,以便他们在出院后能有效的减少对家庭成员、护理人员和公众所造成的照射,特别是未成年人和孕妇。
6.6.2 6.2 诊断中的最优化要求
6.2.1 对患者进行临床核医学诊断中应注意和采取如下最优化措施:
a) 使用放射诊断药物之前,应有确定患者身份、施药前患者的准备和施药程序等有关信息的程序;
b) 对每个诊断程序,应适当考虑与该程序有关的医疗照射指导水平(附录 E);
d)应选择适当的数据采集条件,以便能在达到必要的诊断预期目标下,患者接受的剂量最低。例如,为获取最佳品质影像,应适当选择准直器、能量窗、矩阵尺度、采集时间和放大因子等,以及单光子发射计算机断层成像(SPECT)或正电子发射计算机断层扫描(PET)的有关参数和放大因子;
e)采用动态分析时,为获取最佳品质影像,也应适当选取帧的数量、时间间隔等参数;
f)应确保准直器表面或其他部位不受到放射性污染;
g)在实施诊断后,尤其是在检查后的短时间内,应鼓励患者(特别是儿童)多饮水、多排泄,以加快肾脏排出放射性药物。
6.2.2 采用 Tc-99m 及其放射性药物进行核医学诊断时,可直接采用较小的施用药量和延长成像时间来进行优化,此时通常不需要估算胎儿受照剂量;放射性碘等放射性核素易于穿过胎盘屏障、从而引起胎儿摄入,应按照附录 D 对胎儿受照剂量进行评估,以避免造成事故性照射。
6.6.3 6.3 治疗中的最优化要求
6.3.1 对已接受放射性药物治疗的妇女,应按附录 F 的建议在一段时期内避免怀孕。
6.3.2 已接受 I-131(碘)、P-32(磷酸盐)或 Sr-89(氯化锶)治疗的男性采取避孕措施 4 个月。
6.3.3 在对患者进行核医学治疗时,应采用以下最优化措施:
a) 在使用放射治疗药物之前,应有确定患者身份、施药前患者的准备和施药等有关信息的过程;
b) 在给妇女使用放射性药物前,应询问确认患者是否怀孕或哺乳;
c) 要特别注意防止由于患者的呕吐物和排泄物造成的放射性污染。
6.6.4 6.4 患者剂量管理
6.4.1 应确保给每例患者施用的放射性药物活度与处方量一致,并在服药时记录。
6.4.2 在治疗程序中,应有由具备专门知识的人员对每次治疗的辐射剂量进行评估并予以记录,特别是婴儿和胎儿所受剂量。
6.4.3 需要进行剂量评估时,应按附录 D 建议的方法进行。
6.6.5 6.5 医疗照射指导水平
6.5.1 执业医师应参照医疗照射指导水平(见附录 E),以保证放射性药物施用活度的合理性。
6.5.2 使用指导水平的原则如下:
a) 当患者剂量或施用活度显著低于相应的指导水平,又不能提供有用的诊断信息或给患者带来预期的医疗利益时,应按需要采取纠正行动;
b) 当患者剂量或施用活度显著超出相应的指导水平时,应考虑指导水平是否未达到辐射防护优化,或医学实践活动是否保持在适当良好水平;
c) 附录 E 中给出了一般成年患者的指导水平,也给出了一般儿童的指导水平;这些指导水平是对一般而言的,仅具参考作用,实施诊断检查的医师,应根据患者的体质、病理条件、身体大小和年龄等具体情况,确定合理的施用量。
6.7 7 医疗照射剂量约束
7.1 应向探视者和家庭成员提供有关的辐射防护措施(例如限定接触或接近患者的时间,控制与患者间的距离等)及其相应的放射防护书面指导,并对其所受剂量加以约束,使其在患者的诊断或治疗期间,以及出院后探视者和家庭成员所受的照射处于尽可能低的水平。
7.2附录G中G.1给出了剂量控制的参考值,对知情并自愿扶持患者人员、慰问者和探视者所受的剂量应加以约束,特别是用I-131进行甲亢和甲状腺癌治疗、Sr-89和Re-188缓解骨转移疼痛的患者,在患者诊断检查或治疗期间所受的剂量不超过3mSv。探视已食入放射性药物的患者的婴儿和儿童所受剂量应约束在1mSv以下。
7.3 对接受了I-131 治疗的患者,其体内放射性活度降至低于400 MBq 之前不得出院,对接受其他放射性药物治疗的患者仅当患者体内放射性活度低于附录G中G.2要求时才能出院。患者体内活度检测控制应按G.3推荐的方法进行。
7.4 对甲亢和甲状腺癌患者,出院时应按附录G中G.4给出接触同事和亲属及到公众场所的合理限制和有关防护措施(限制接触时间及距离等)的书面建议。
6.8 8 异常医疗照射的调查与处理
a) 任何放射性核素治疗中,出现患者或靶组织辨识错误,或使用的药物、剂量,或剂量的分次给予情况与执业医生处方有实质性不同;
b) 任何诊断用药物的施用量远远大于处方值,或多次重复照射,或大大超过设定的指导水平;
c) 任何设备故障、事故、错误或意外事件,使患者受到与诊疗计划不一致的照射,或受到其他非正常发生的潜在照射。
8.2 针对上述异常医疗照射,核医学单位应进行以下调查与处理:
b) 为防止同类事件再次发生所需的纠正措施,并立即组织实施所有纠正措施;
c) 调查后应尽快向监管机构提交书面报告,说明事件的原因,以及上述 a) 和 b) 的内容;
6.9 9 记录和档案
a) 每个患者所施用的放射性药物名称、类型、给药途径、分次给予的方式及其施用活度;
b) 医学研究中志愿者所施用的放射性药物名称、类型、给药途径、分次给予的方式及其施用活度。
9.2 核医学单位应建立放射性药物使用档案,其内容包括放射性药物来源及主要特性、质量检测、储存、使用过程和放射性废物处置等的记录。应记录如下放射性药物的主要特性:
a) 对颗粒状放射性药物,严格控制其颗粒的大小。例如,使用大聚体白蛋白(MAA)时,为避免引起肺动脉栓塞应将其 90%的颗粒大小控制在 10μm90 μm 范围,最大不应超过 150 μm。
b) 放射性药物产品应有热源反应结果、放射化学纯度分析结果和灭菌效果等的标识和说明。此外,还应标识以下内容:
2) 总放射性活度;
3) 活度测量时间;
4) 制造商名称和地址;
5) 有效期;
8) 其他相关参数。
7 附录A(规范性附录)
医疗照射的质量控制
7.1 A.1 医疗照射质量保证大纲
医疗照射质量保证大纲至少应包括以下的内容:
a) 对新或维修过的显像器件和辐照装置,使用前应测量其相关的物理参数,并且以后对其进行定期测量;
c) 书面记录和操作的规范化程序(例如患者的病史和体征,诊断摘要,适应证和禁忌证等);
d) 确认使用的放射性药物及其使用程序与执业医师开具的处方相一致的验证程序;
7.2 A.2 管理制度和操作流程
管理制度和操作流程至少应包括以下内容:
a) 诊疗申请及处方程序(包括患者的病史和体征,诊断摘要,适应症和禁忌证等内容);
b) 放射性药物使用程序(包括可靠的施药程序及药物施用量质控,患者信息及身份识别等内容);
c) 临床工作程序(包括放射性药物制备及转运,临床环境,患者的运送和准备,设备操作,采购规程和废物处理等内容);
d) 技术培训及经验收集程序(包括所有相关人员的培训和经验收集等内容);
e) 数据分析和处理程序(包括处理规程,设备性能,数据精确度和完整性等内容);
f) 结果报告程序(包括数据和图像分析,结果和进一步的建议等内容)。
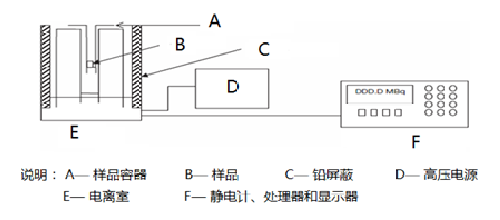
7.3 A.3 放射性药物施用量质控检测
应用活度计对放射性药物施用量进行抽样质控检测,图A.1 是的典型的活度计测量装置示意图。除定期按国家相关规定对其校准外,每周还应对活度计的稳定性检查一次。
9 附录C(规范性附录)
C.1 对儿童施用放射性药物时,其施用量用公式(C.1)计算。
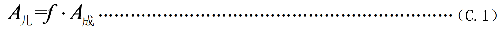
式中:
f ——成人施用量施用于儿童的分数,其值列于表C.1;
A成——成人放射性药物施用量,单位为兆贝可(MBq)。
表 C.1 成人施用量施用于儿童的分数建议

表C.1 中f值是一个范围值,具体取值可参看表C.2中,单位施用量引起的不同年龄有效剂量取值,即引起非成年人剂量大的f值应向小的方向取值。

表 C.2(续)

10 附录D(资料性附录)
10.1 D.1 临床核医学中患者接受剂量的估算
a) 临床核医学诊疗中,用放射性活度施用量(A)与单位施用量的患者不同器官所接受的吸收剂量(dT)的乘积来估算患者不同器官的剂量(DT),即:
![]()
式中:
DT——患者 T 器官所受的吸收剂量,单位为毫戈(mGy);
A——放射性活度施用量,单位为兆贝可(MBq);
dT——单位施用量下患者 T 器官所接受的的吸收剂量,单位为毫戈每兆贝可(mGy/MBq)。
b) 在核医学患者剂量估算中,用有效剂量对全身接受剂量进行综合评价,有效剂量 E 用公式(D.2)进行计算:

式中:
dE——单位施用量引起的患者的有效剂量,单位为毫希每兆贝可(mSv/MBq)。
在表 D.1~D.4 中分别列出了成人(>14 岁)、少儿(≤14 岁且>8 岁)、幼儿(≤8 岁且>3 岁)
和婴儿(≤3 岁)患者的 dT和 dE的值,这些建议值来自 ICRP Publication 53、CRP Publication 80 和 ICRP Publication 106。
注1:本附录各表中仅列出少数器官,不能用这些少量器官的数据估算有效剂量,因为接受剂量最大的器官有可能未列出,这样估算的结果可能会有数量级的差异。如果要估算有效剂量,请参看 ICRP 53,80、和 106 号出版物。
注2:在进行核医学患者剂量估算时,应该用 ICRP 53、ICRP 80 和 ICRP 106 号出版物的方法及参数,不应使用 GB 18871-2002 附录 C 中表 C.3 的 e(g),后者是连续摄入模式的估算,它仅用于职业照射。
10.2 D.2 临床核医学中胎儿接受剂量的估算
服用放射性药物的怀孕母亲所致的胎儿的有效剂量,EF用公式(D.3)估算:
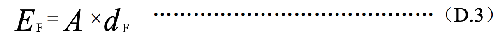
式中:
A——放射性活度施用量,单位为兆贝可(MBq);
dF——怀孕母亲服每 MBq 放射性药物致使胎儿的有效剂量值,单位为毫希每兆贝可(mSv/MBq),其值列在表 D.5 中。
当用公式(D.3)估算的胎儿剂量超过 100mGy 时,应建议患者终止怀孕或避免怀孕。
表 D.1 临床核医学中成人单位施用量患者接受的器官吸收剂量(dT)及有效剂量(dE)
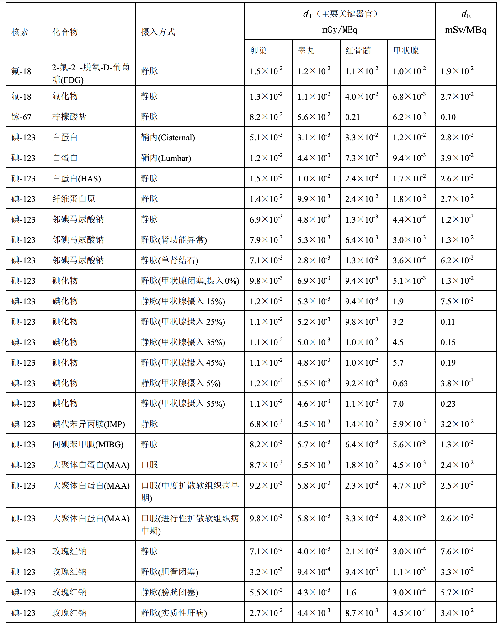
表 D.1(续)
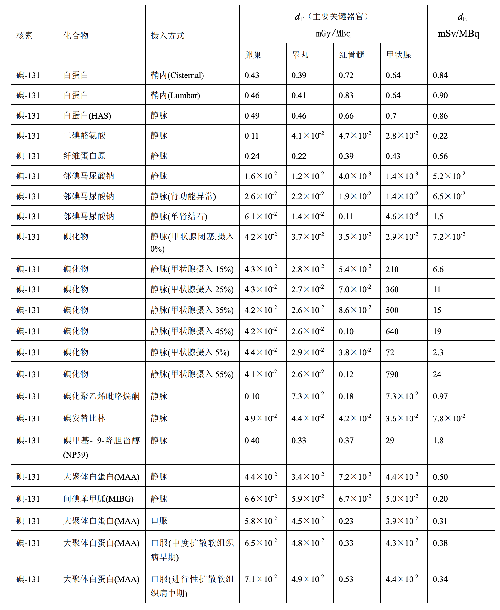
表 D.1(续)

表 D.1(续)

表 D.1(续)
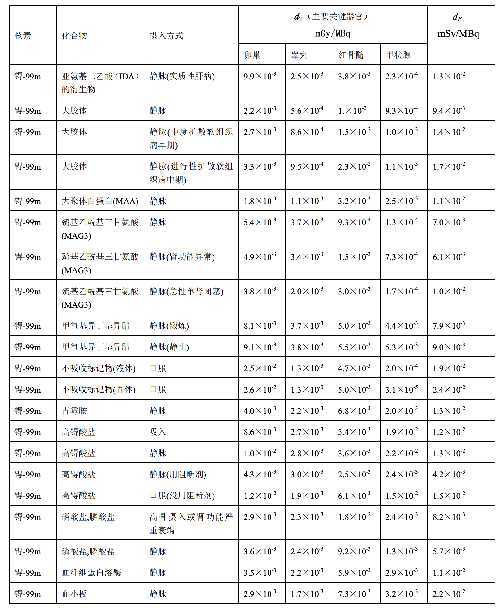
表 D.1 (续)
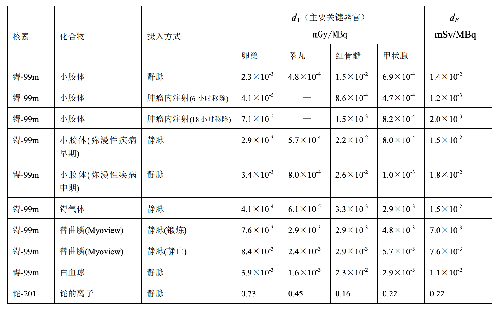
表 D.2

表 D.2 (续)

表 D.2 (续)

表 D.2 (续)
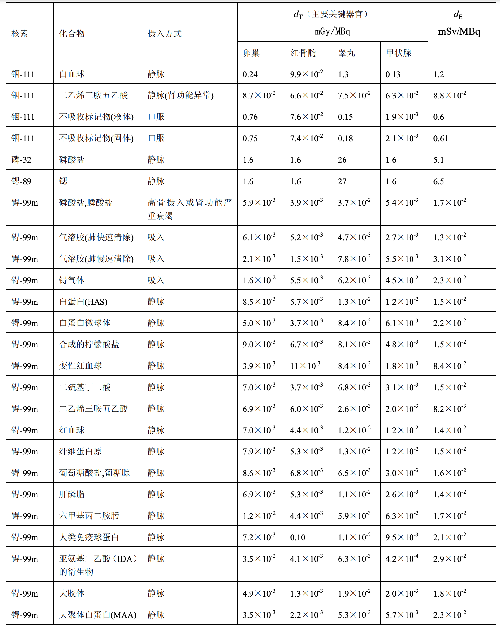
表 D.2 (续)
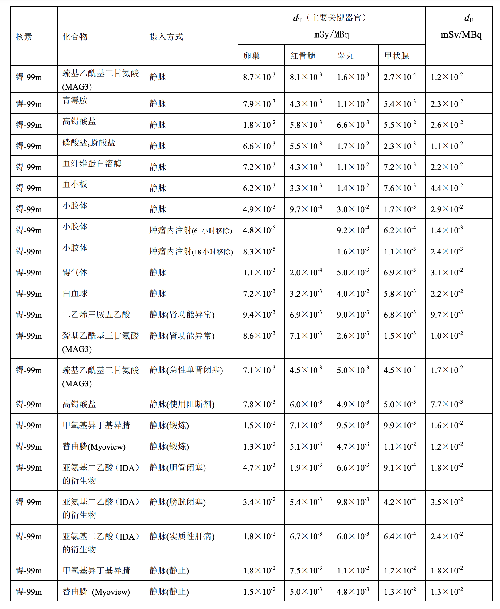
表 D.2 (续)
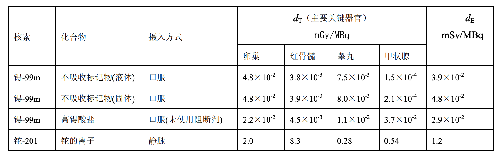
表 D.3
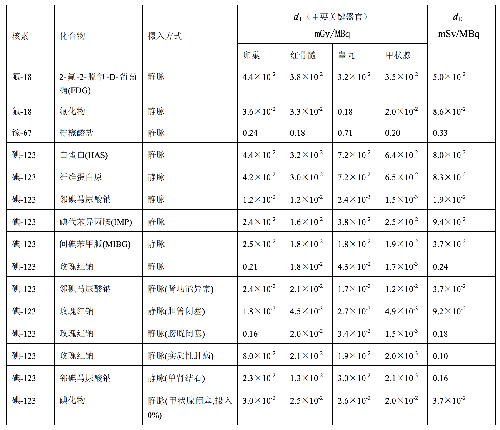
表 D.3 (续)
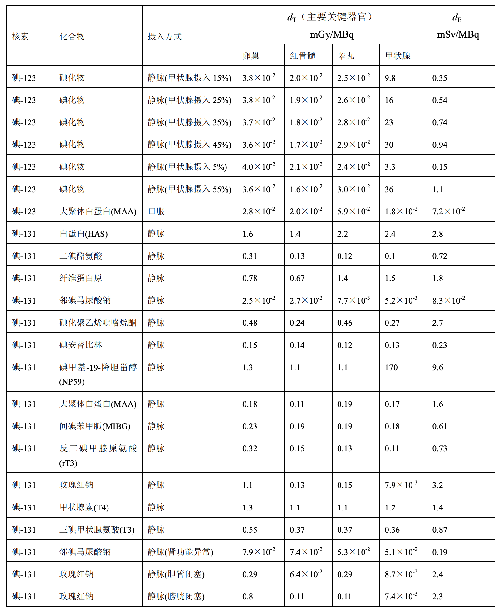
表 D.3 (续)
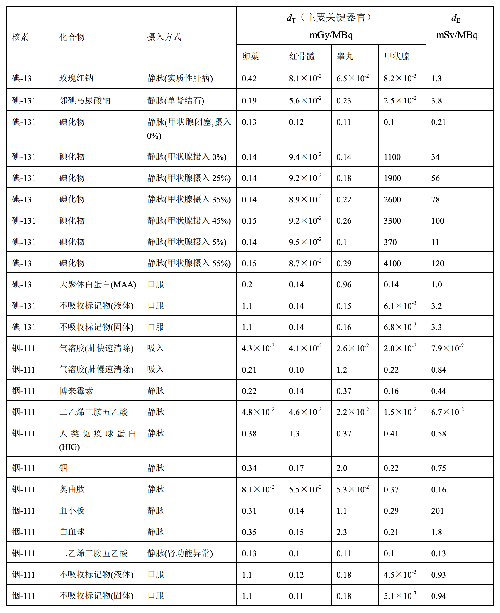
表 D.3 (续)
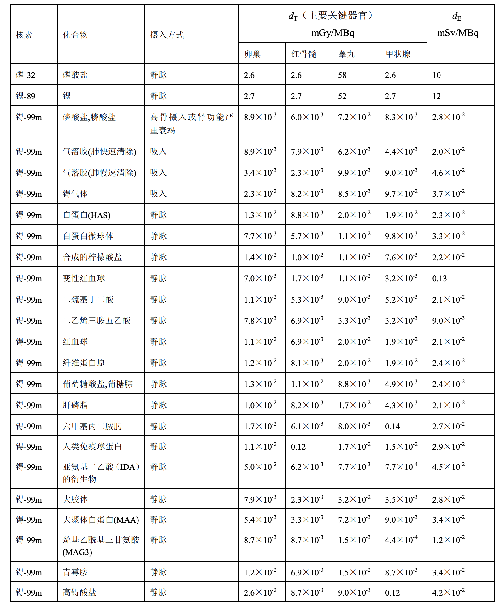
表 D.3 (续)

表 D.4 临床核医学中婴儿单位施用量患者接受的器官吸收剂量(dT)及有效剂量(dE)
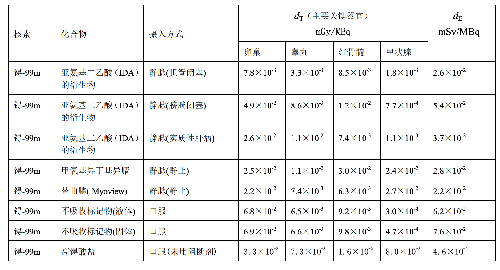
表 D.4 (续)
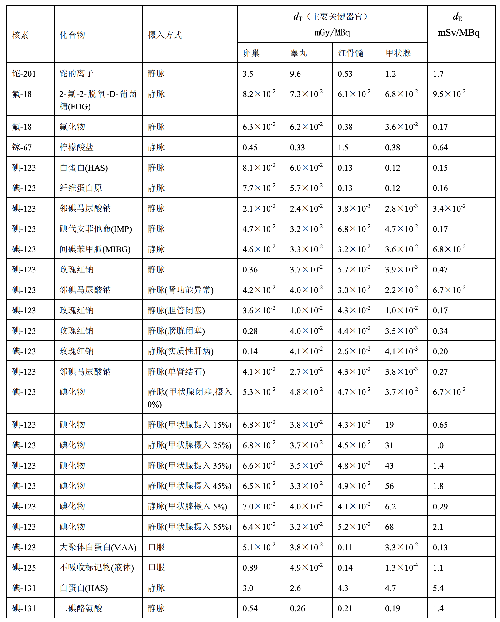
表 D.4 (续)
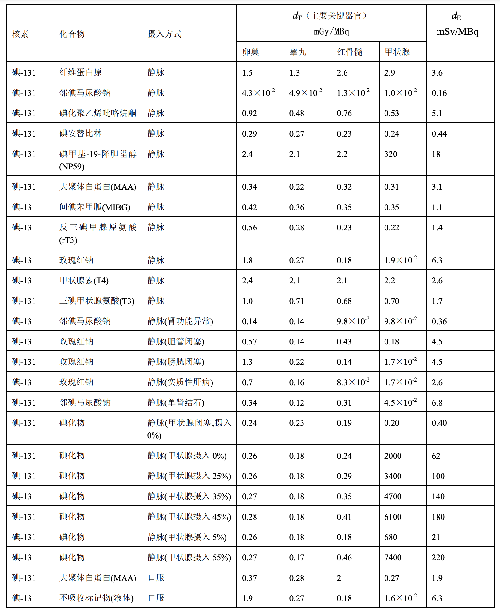
表 D.4 (续)

表 D.4 (续)
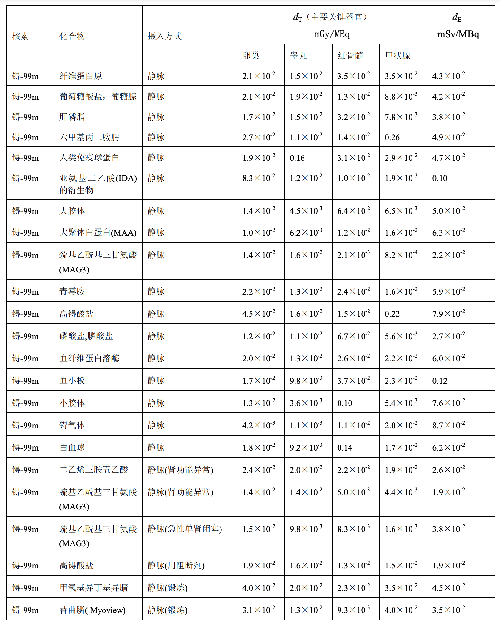
表 D.4 (续)
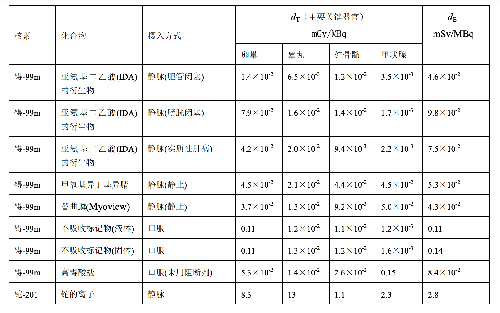
表 D.5

表 D.5 (续)

11 附录E(规范性附录)
医疗照射的指导水平
11.1 E.1 成人的医疗照射指导水平
表 E.1 给出了典型成年受检者各种常用放射性药物施用量的导水平。
表 E.1 典型成年患者核医学诊断过程放射性药物施用量的指导水平
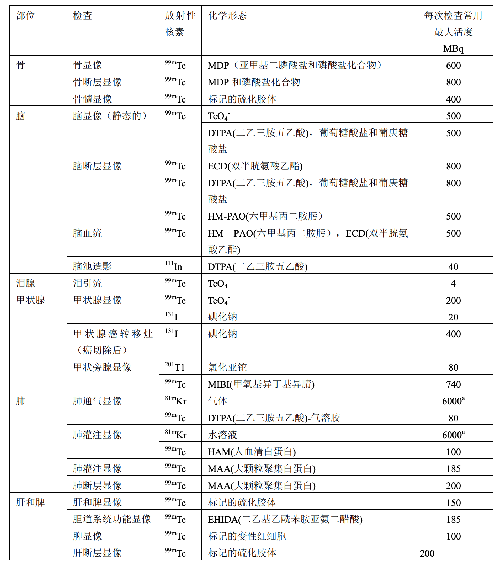
表 E.1(续)
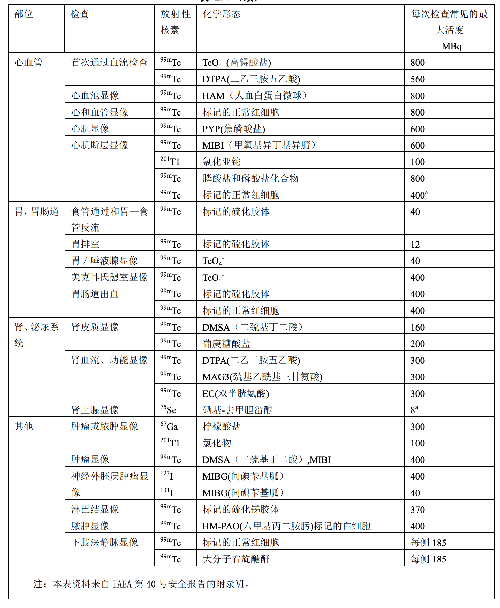
原则上,儿童的施用量指导水平可以用成人的指导水平乘以成人施用量用于儿童的分数 f(附录 C表 C.1)得到,因此,儿童的指导水平随体重而变化。表 E.2 是一个儿童的指导水平的举例,资料来自2010 North American Consensus Guidelines。
12 附录F(规范性附录)
接受临床核医学治疗妇女避免怀孕的时期建议
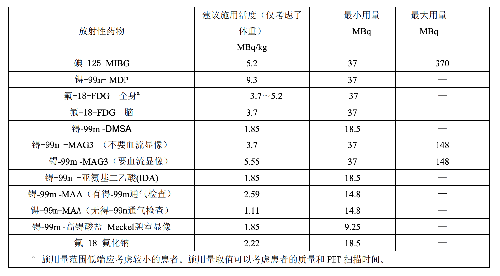
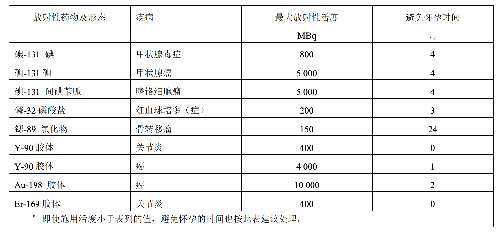
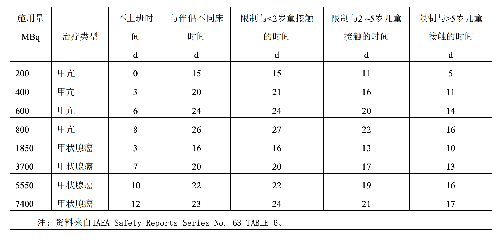
对于使用下述放射性核素治疗后的妇女,表 F.1 给出了治疗用最大活度和治疗后避免怀孕时间的建议。此处采用的建议值来自 2005 年 IAEA 40 号安全报告附录Ⅴ之表 20。
表 F.1 放射性核素治疗用最大活度和治疗后避免怀孕时间的建议 a
13 附录G(规范性附录)
13.1 G.1 医疗照射剂量约束控制方法
13.1.1 G.1.1 通用准则
患者家人或探访者与接受临床核医学诊疗的患者接触,应按如下方法控制接受的剂量:
a)孕妇及2岁以下儿童应尽量避免接触接受临床核医学诊疗的患者;
b)3-10岁儿童每次接触的剂量D3-10应满足如下不等式:

式中:
D3-10——3-10 岁儿童每次接触的剂量,单位为毫希(mSv)。
c)10岁以上人员每次接触的剂量D>10应满足如下不等式:
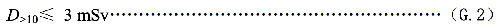
式中:
D>10——10岁以上人员每次接触的剂量,单位为毫希(mSv)。
一般不应超过1mSv,即使10岁以上的人员每次接触的剂量也不应超过3mSv。
13.1.2 G.1.2 接近患者人员的剂量估算方法
D3-10和D>10均按如下方法估算:
a)离患者距离≥3m的情况:
当患者家人或探访者与患者接触的距离≥ 3m 时,此时可用公式(G.3)估算其剂量:
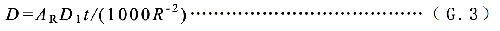
式中:
AR——放射性药物施用到患者后,某一时刻体内的放射性活度,单位为兆贝可(MBq);
D1——患者体内单位放射性活度所致体外1m处的剂量率,单位为微希平方米每小时兆贝可(μSv∙m2(h∙MBq)-1),不同放射性药物的D1推荐值见表G.1;
t ——接触时间,单位为小时(h);
b)离患者距离<3m 的情况:
患者家人或探访者与患者接触的距离<3m,此时若按反平方估算误差会较大,为此应按下式估算:

式中:
AR——放射性药物施用到患者后,某一时刻体内的放射性活度,单位为兆贝可(MBq);
D1——患者体内单位放射性活度所致体外1m处的剂量率,单位为微希平方米每小时兆贝可(μSv∙m2(h∙MBq)-1),不同放射性药物的D1推荐值见表G.1;
t ——接触时间,单位为小时(h);
尽管公式(G.3)和公式(G.4)的估算误差较大,但对进行是否超过剂量约束的判断还是可行的。
表G.1 患者体内单位放射性活度所致体外1m处的周围剂量当量率
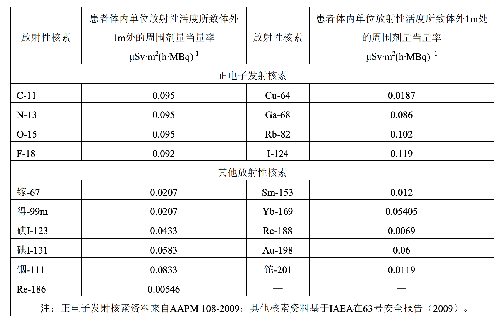
患者体内放射性活度(A R)用公式( G.5)估算。
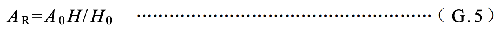
式中:
AR——测量时刻t 滞留的的放射性活度,单位为兆贝可(MBq);
A0——施用给患者的放射性初始活度,单位为兆贝可(MBq);
H0——施药后首次测量的周围剂量当量率,单位为微希每小时(μSv/h);
H——时刻t 测量的周围剂量当量率,单位为微希每小时(μSv/h)。
H0和 H用 图 G.1的方法进行规范的测量。应在给患者施用放射性核素后、还没有任何排泄以前,尽快地用防护巡测仪进行首次周围剂量当量率(H0)测量;到需关注的某一时刻,在这个固定位置上,用上述防护巡测仪(而且校准因子相同)再次测量周围剂量当量率(H)。将相应的值带入公式(G.5)就可以得到关注时刻患者体内放射性活度(AR) 。
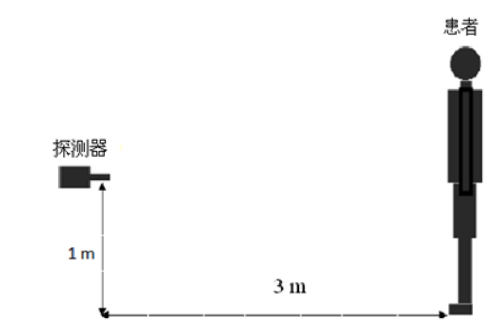
图 G.1 探测器与患者的相互位置
13.2 G.2 患者出院的体内放射性活度要求
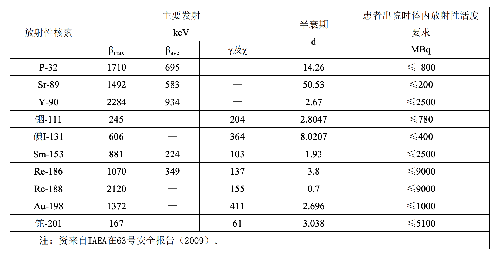
为确保放射治疗患者出院后,不至于使接触患者的家庭成员及公众超过相关的剂量约束或剂量限值,放射治疗患者出院时体内放射性活度应符合表G.2的要求。
表G.2 放射治疗患者出院时体内放射性活度的要求
13.3 G.3 患者出院时体内放射性活度控制方法
13.3.1 G.3.1 有γ及χ发射的放射性核素
当施用给患者的是有γ及χ发射的放射性核素,则可采用G.1.2中(3)款的方法检测患者体内的放射性活度。
13.3.2 G.3.2 无γ及χ发射的放射性核素
当施用给患者的是无γ及χ发射的放射性核素,则可采用G.1.2中(3)款类似方法检测患者体内的放射性活度,这时的距离可减少到30cm,测量仪器改为表面污染仪就可以了。
13.4 G.4 出院患者辐射防护书面指导内容
对甲亢和甲状腺癌患者出院时的辐射防护书面指导至少应包括以下内容:
a)与同事和亲属的接触应符合表G.3的限制;
当出院时患者体内的碘I-131放射性活度为400MBq时,按表G.1,这时离患者1m处的周围剂量当量率=400╳0.0583=23.3 μSv/h。显然,这样情况下参加1天以上的跟团旅游会给其他人员带去超过国家公众剂量限值的照射,为此这类患者的出行时间及旅游方式应符合表G.4的要求。
表G.3 甲亢和甲状腺癌患者出院后与同事和亲属接触的相关限制

14 参考文献
[1] IAEA,Quality Management Audits in Nulear Medicine Practices,2008
[2] IAEA Safety Reports Series No. 63,Release of Patients After Radionuclide Therapy,2009
[3] IAEA Safety Reports Series No. 40,Applying Radiation Safety Standards in Nuclear Medicine 2005
[4] IAEA Technical Reports Series No. 454,Quality Assurance for Radioactivity Measurement in Nuclear Medicine,2006
[5] IAEA,Nuclear Medicine Resources Manual,2006
[6] AAPM Task Group 108-2009: PET and PET/CT Shielding Requirements
[7] ICRP Publication 80 addendum to ICRP 53,, Radiation Dose to Patients from Pharmaceuticals. Annals of the ICRP. Vol 28 No 3 1998
[8] ICRP Publication 86,Prevention of Accidental Exposures to Patients undergoing Radiation Therapy, Annals of the ICRP. Vol 30 No 3, 2000
[9] ICRP Publication 88(Corrected Version), Doses to the Embryo and Fetus from Intakes of Radionuclides by the Mother , Annals of the ICRP.Vol 31 No 1-3, 2001
[10] ICRP Publication 94, Release of Patients after Therapy with Unsealed Radionuclides Annals of the April 2005
[11] ICRP Publication 105,Radiological Protection in Medicine,2007
[12] ICRP Publication 106 Radiation Dose to Patients from Radiopharmaceuticals: Addendum 3 to ICRP Publication 53, Ann. ICRP 38(1-2), 2008
[13] Michael J. Gelfand1, Marguerite T. Parisi2, and S. Ted Treves3,Pediatric Radiopharmaceutical Administered Doses:2010 North American Consensus Guidelines
16 《临床核医学患者防护要求》解读
为加强放射诊疗工作的管理,保证医疗质量和医疗安全,保障放射诊疗工作人员、患者和公众的健康权益,依据《中华人民共和国职业病防治法》、《放射性同位素与射线装置安全和防护条例》、《放射性药品管理办法》和《医疗机构管理条例》等法律、行政法规的规定,我国2006年发布了《放射诊疗管理规定》,2012年发布了《临床核医学的患者防护与质量控制规范》(GB 16361—2012)。《临床核医学患者防护要求》由GB 16361—2012转化而来。与GB16361—2012相比主要变化是:将原标准名称“临床核医学的患者防护与质量控制规范”修改为“临床核医学患者防护要求”;因核医学设备质量控制内容已列入相关标准中,且一般性药物控制不属于本标准的范围,故删除设备质量控制和一般性药物质量控制的内容;根据国际原子能机构的40号安全报告《辐射安全标准在核医学中的应用》和63号安全报告《放射性核素治疗后患者出院管理》的规范和要求,增加了核医学患者出院管理的具体方法、胎儿剂量计算方法、儿童医疗照射指导水平、探视者和家庭成员剂量约束规定及控制方法等有效加强患者、探视者和家庭成员及公众防护的具体方法和规范。