3 基本信息
ICS 11.020
CCS C 50
中华人民共和国卫生行业标准 WS/T 220—2021《凝血因子活性测定技术标准》(Technical standard for coagulation factor activity assay)由中华人民共和国国家卫生健康委员会于2021年08月27日《关于发布《凝血因子活性测定技术标准》等2项推荐性卫生行业标准的通告》(国卫通〔2021〕9号)发布,自2022年01月01日起实施,代替WS/T 220—2002,WS/T 220—2002同时废止。
4 发布通知
关于发布《凝血因子活性测定技术标准》等2项推荐性卫生行业标准的通告
国卫通〔2021〕9号
现发布《凝血因子活性测定技术标准》等2项推荐性卫生行业标准,编号和名称如下:
WST 220—2021 凝血因子活性测定技术标准(代替WS/T 220—2002)
WST 785—2021 人类白细胞抗原基因分型检测体系技术标准
上述标准自2022年1月1日起施行,WS/T 220—2002同时废止。
特此通告。
国家卫生健康委
2021年8月27日
5 前言
本标准代替 WS/T 220-2002《凝血因子活性测定总则》,与WS/T 220-2002相比,主要技术内容变化如下:
a) 将“总则”更改为“技术标准”,细分了原则,并将 2002 年版的有关内容精简更改后纳入(见附录,2002 年版的 11.1、11.2、11.3、11.4);
b) 调整技术标准内容框架结构,根据检测流程进行技术指标分层细化;
c) 增加了对检测项目室内质控和室间质评的技术指标参数设定(见5.6.1、5.6.2、5.6.3、5.6.4、5.7.1、5.7.2,2002年版10.1、10.2、10.3、10.4);
d) 增加了两种新的测定方法(见5.1.1.2、5.1.1.3,2002年版8.1);
e) 增加了性能验证技术指标设定(见5.4.1、5.4.2、5.4.3、5.4.4)。
本标准由国家卫生健康标准委员会临床检验标准专业委员会负责技术审查和技术咨询,由国家卫生健康委医管中心负责协调性和格式审查,由国家卫生健康委医政医管局负责业务管理、法规司负责统筹管理。
本标准起草单位:上海交通大学医学院附属瑞金医院、国家卫生健康委临床检验中心、中国医学科学院北京协和医院、中国医学科学院血液病医院。
本标准主要起草人:王学锋、彭明婷、赵永强、杨仁池、戴菁、周文宾。
6 标准正文
凝血因子活性测定技术标准
6.1 1 范围
本标准规定了用一期法检测凝血因子(Ⅱ、Ⅴ、Ⅶ、Ⅷ、Ⅸ、Ⅹ、Ⅺ、Ⅻ)活性测定的技术要求。由于方法学不一致,本文件不涉及纤维蛋白原检测和凝血因子XIII的检测。本标准适用于开展凝血因子活性检测的医学实验室,用于规范相应的检测过程和质量控制。
6.2 2 规范性引用文件
下列文件对于本标准的应用是必不可少的。凡是注日期的引用文件,仅所注日期的版本适用于本标准。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本标准。WS/T 359 血浆凝固实验血液标本的采集及处理指南
6.3 3 术语与定义
下列术语和定义也适用于本文件。
3.1
血浆与凝血活酶试剂(例如,组织因子)和氯化钙反应后发生凝固所需要的时间。[来源:WS/T 359-2011,2.1]
3.2
活化部分凝血活酶时间 activated partial thromboplastin time, APTT
血浆与适量的氯化钙(CaCl2)、部分凝血活酶试剂盒接触因子激活剂(如白陶土)反应后发生凝固所需要的时间。
[来源:WS/T 359-2011,2.2]
3.3
定标曲线 calibration curve
参考曲线
定量反映凝血因子活性与纤维蛋白形成所需时间之间的相互关系的曲线。
3.4
定标血浆 calibration plasma
已知凝血因子活性的枸橼酸钠抗凝的正常混合血浆,用于制备定标曲线。
3.5
乏因子血浆 factor-deficient plasma
3.6
质控血浆 control plasma
源于人或动物血,或者人工制成的新鲜、冰冻或冻干的血浆,用于质量控制。
3.7
缓冲液 buffered solution
具备缓冲酸碱能力的液体,如Owrens缓冲液、咪唑缓冲液等。
3.8
用于检测或评估特定物质存在与否,或对血液、体液中的物质进行定性、定量分析的一组装置。检测系统包括操作说明和所有的仪器、设备、试剂及(或)获得检测结果所需的物品。
6.4 4 检验前过程
6.4.1 4.1 标本采集
依照 WS/T 359的要求进行标本采集。选择塑料针筒或者负压采血系统,建议成年人血样采集使用19G或21G针头,婴幼儿血样采集使用22G或23G针头,静脉穿刺采血时,应规范采血流程,一次穿刺成功,尽量避免引起凝血因子激活的操作。若患者的血细胞比容异常升高(Hct≥55%),应按WS/T359推荐的公式进行抗凝剂比例的调整。
标本采集前患者应处于平静和空腹状态,剧烈运动和应激反应可使因子Ⅷ活性增加(其作用可持续30 min);脂血可使因子Ⅶ活化,同时干扰以光学法为原理的凝血仪的检测结果,此时可改用手工或磁珠原理凝血仪进行测定。
6.4.2 4.2 标本运送、处理和保存
4.2.1 标本采集后应确认无血凝块存在,采集后宜在1 h内送检,采用规定的离心速度和离心时间(室温、1500 g、不少于15 min)分离血浆,以获得乏血小板血浆(血小板计数<10 ×109/L),4h内完成血浆标本检测。
4.2.2 依照 WS/T 359的要求在常温下进行标本运送,标本应在采集后尽快送检(若不能及时检测,应在分离血浆后置于4℃冰箱4 h内完成检测)。冰冻血浆在-20℃条件下最多可保存2周,在-70℃条件下最多可保存6个月。
4.2.3 若使用冷藏标本,检测前应将标本于室温放置15 min~20 min使其恢复至室温。4.2.4 若使用冰冻血浆标本,应将其置于37℃水浴快速复融至少4 min~5 min,检测前标本应充分混匀。
6.4.3 4.3 标本拒收标准
WS/T 220—20213实验室应制订不合格标本的拒收标准,包括(但不限于以下内容):
a) 申请单和试管标签上的信息不一致、试管条码信息错误、试管标签或试管条码脱落;
c) 当标本存在凝块、溶血、抗凝剂使用错误或采血量不当(与标示量相差超过±10%)时。
6.4.4 4.4 标本误差来源
a) 采血量不当(与标示量相差超过±10%);
b) 使用非规定的抗凝剂(如EDTA盐或草酸盐)、抗凝剂的浓度、用量不准确;
e) 采血器或贮血管不洁,或受到污染;使用非规定、不适当的标本采集管;
f) 血细胞比容高于或等于55%;
g) 急性炎症反应、纤维蛋白原升高或纤维蛋白原异常可使采用PT途径测定的凝血因子活性不准确;
6.5 5 检验过程
6.5.1 5.1 检测系统
6.5.1.1 5.1.1 检测方法原理
6.5.1.1.1 5.1.1.1 一期法检测
5.1.1.1.1 检测原理:基于检测待测标本对乏因子血浆所致的凝固时间(PT 或APTT)延长的纠正能力。将稀释后的待测血浆与乏因子血浆混合后进行 PT 或 APTT 检测,检测结果与待测血浆中的凝血因子活性呈负相关。通过使用已知凝血因子活性的血浆进行系列稀释并与乏因子血浆混合后进行PT 或APTT检测建立的定标曲线,可以得出待测血浆中相应凝血因子的活性。一期法检测是目前最常用的凝血因子活性测定方法。
5.1.1.1.2 基于 PT 检测的凝血因子:因子Ⅱ、Ⅴ、Ⅶ、Ⅹ。
5.1.1.1.3 基于 APTT 检测的凝血因子:因子Ⅷ、Ⅸ、Ⅺ与Ⅻ。
6.5.1.1.2 5.1.1.2 二期法检测
该方法适用于因子Ⅷ/Ⅸ活性检测,以因子Ⅷ活性检测为例,其原理为:基于检测因子Ⅷ作为辅因子与因子Ⅸa形成复合物活化因子Ⅹ的能力,通过检测生成的因子Ⅹa的量可计算因子Ⅷ的活性。该实验分为两步进行,第一步:待测标本与含有磷脂、钙离子、因子Ⅸa以及因子Ⅹ的试剂溶液进行孵育后生成因子Ⅹa;第二步再加入过量的凝血酶原和纤维蛋白原,检测纤维蛋白凝块形成的时间。测得的凝固时间可以通过查对已知凝血因子活性的定标曲线或代入回归方程,得到凝血因子活性。
6.5.1.1.3 5.1.1.3 发色底物法检测
该方法是二期法检测的改进方法,在因子Ⅷ活性检测时使用。第一步:待测标本与含有磷脂、钙离子、因子Ⅸa以及因子Ⅹ的试剂孵育后生成因子Ⅹa;第二步加入因子Ⅹa的发色底物进行检测,因子Ⅹa可作用在发色底物S2765,使其释放对硝基苯胺(paranitroaniline,pNA),后者可在405 nm波长条件下通过读取吸光度值计算该物质的生成量,通过计算转换为凝血因子活性。
6.5.1.2 5.1.2 检测系统选择
5.1.2.1 实验室宜选用仪器与试剂配套的检测系统。使用非配套检测系统时,应确认该系统是否能满足性能验证要求。
5.1.2.2 实验室在选择检测系统时,应考虑的因素(但不限于以下内容)包括:
a) 临床标本性状:黄疸、脂浊等影响光散射强度的标本,适宜选择物理学检测原理的检测系统(如磁珠法)进行测定;
b) 标本数量与检测速度:检测系统能够在规定时间内完成常规标本和急诊标本的测定。
6.5.2 5.2 试剂和耗材
6.5.2.1 5.2.1 APTT 试剂
不同APTT试剂由于激活剂的不同而对凝血因子活性检测的敏感性存在差异。检测凝血因子缺乏时,宜选用对凝血因子缺乏有高敏感性的APTT试剂(可检出凝血因子活性<30%的标本,包括凝血因子Ⅷ、Ⅸ、Ⅺ等)。针对怀疑存在狼疮抗凝物的标本,宜使用对磷脂不敏感的APTT试剂盒。实验室在更换APTT试剂批号时,应进行新旧试剂的比对:根据验证标本的目标水平(验证标本应尽量覆盖检测项目的可报告范围,并至少包含正常水平和异常水平)、各水平的确定临界值、不精密度值等参数来确定所需标本数,分别采用新旧试剂进行检测,计算偏差和平均偏差绝对值,并与拒绝限进行比较,判断批号间验证是否通过。
6.5.2.2 5.2.2 PT 试剂
不同PT试剂中凝血活酶因其来源不同(可来自人、兔、牛、猴等脑或其他组织)而具有不同的敏感度。应选择敏感度高(ISI接近1)的凝血活酶试剂,实验室在更换凝血活酶试剂时,应对其ISI值进行评估。
6.5.2.3 5.2.3 乏因子血浆
乏因子血浆应符合以下要求:待测的目标凝血因子活性低于0.01 IU/mL(1%),其他凝血因子活性高于0.5 IU/mL(50%),纤维蛋白原含量高于1.0 g/L。实验室应对每个批次的乏因子血浆进行检测,以确保所用的乏因子血浆质量符合上述要求。乏因子血浆应在冷藏(冻干形式)或冰冻(贮存-70℃冰箱)条件下妥善保存。
6.5.2.4 5.2.4 定标血浆
通常使用商品化的标准血浆或校准血浆,其标示值需溯源至国际标准物质(如世界卫生组织发布的国际标准品)。若实验室自行制备定标血浆,应至少使用20例以上健康志愿者(男女各半,年龄18岁~55岁,六个月内未服用任何药物,女性未处于妊娠期或月经期)的混合血浆。血浆制备时需进行两次离心,将第一次离心获得的乏血小板血浆的上层2/3体积转移入加塞塑料试管进行第二次离心(室温、1500g、不少于15 min),注意不要使用第二次离心后的底部血浆,以确保充分去除血小板,以国际标准物质作为溯源标准确定其凝血因子活性水平,并保证凝血因子的活性在(1±0.2)IU/mL。
6.5.2.5 5.2.5 试剂误差来源
试剂误差来源包括(但不限于以下内容):
a) 试剂已被污染;
b) 配制的试剂未采用 I 级试剂级水或厂家指定用水、复溶时使用非规定的稀释液、复溶时稀释液加量不准;
c) 在运输或贮存过程中,因处置不当(如温度等因素)而导致试剂变质;
6.5.3 5.3 定标曲线制作
6.5.3.1 5.3.1 正常值定标曲线
5.3.1.1 采用全自动血液凝固分析仪进行凝血因子活性检测时,可按照仪器生产厂商的要求预先设定参考血浆的稀释比例并使用配套参考血浆制作定标曲线。参考血浆的稀释比例应至少包括1/10、1/20、1/40 和 1/80 四个水平。采用手工法或半自动血液凝固分析仪进行检测时,需根据不同比例稀释标本的PT 或 APTT 检测结果与对应的稀释比例在半对数或双对数坐标纸上手工绘制定标曲线。(示例见附录A)5.3.1.2 定标曲线的线性回归方程的 r 值应在 0.998~1.000,斜率应在0.9~1.1。5.3.1.3 频率:对于采用手工法或半自动方法进行凝血因子活性检测时,每批次均需建立本次的定标曲线;全自动检测方法在试剂批号更换、仪器设备调整、室内质控失控等情况下需重新建立定标曲线。
6.5.3.2 5.3.2 低值定标曲线
针对低值标本(凝血因子活性水平<5%)应建立低值定标曲线,定标血浆可按照1/20、1/40、1/80······的比例进行稀释,其余要求同正常定标曲线的制备。
6.5.4 5.4 性能验证
6.5.4.1 5.4.1 性能验证一般要求
5.4.1.1 新的检测系统用于临床检测前,依据厂家介绍的要求进行校准和性能验证,至少应包括批内精密度、批间精密度、正确度和可报告范围等。
5.4.1.2 验证周期:在更换设备、组件以及试剂时需要进行性能验证。
6.5.4.2 5.4.2 重复性
重复性又称批内精密度,是以连续检测结果的变异系数(CV)为评价指标。重复精密度的验证方法:至少使用两个浓度水平(包含正常和异常水平)的新鲜临床标本或质控物进行检测,每个标本按常规方法重复检测 11 次,剔除第 1 次检测结果,计算后 10 次检测结果的变异系数。内源性凝血因子(APTT途径) 和外源性凝血因子(PT 途径)的正常标本和异常标本的 CV 应均≤10%。
6.5.4.3 5.4.3 期间精密度
期间精密度又称为批间精密度,以室内质控检测结果的变异系数为评价指标。批间精密度的验证方法:至少使用两个浓度水平(包含正常和异常水平)的质控物或临床标本,在标本检测当天至少进行1次室内质控,剔除失控数据后按批号或按月份,计算累计在控数据 20 次结果的变异系数。内源性凝血因子(APTT 途径) 和外源性凝血因子(PT 途径)的正常标本和异常标本的CV 应均≤15%。
6.5.4.4 5.4.4 正确度
正确度以国际标准物质或商业校准物实际检测结果与理论值的偏倚(Bias)为评价指标。实验室应尽可能使用有证标准物质(如国际标准物质或国家标准物质)进行正确度验证,在无法得到上述标准物质的情况下,可使用商业标准物质。正确度的验证方法:将标准物质稀释至预期浓度水平(如医学决定水平)并至少重复检测10次,计算检测结果的均值与理论值的百分偏差,要求百分偏倚(Bias)应≤15%。
6.5.5 5.5 检测程序
6.5.5.1 5.5.1 标准操作程序的建立与实施
实验室应依照《医疗机构临床实验室管理办法》、本文件和仪器试剂生产厂商的操作说明制定各检测项目的标准操作程序(Standard Operation Procedure,SOP)文件,并严格按照SOP 文件的要求进行操作。
6.5.5.2 5.5.2 检测方法的选择
因子Ⅱ、Ⅴ、Ⅶ、Ⅷ、Ⅸ、Ⅹ、Ⅺ、Ⅻ的活性均可使用一期法进行检测,因子Ⅷ/Ⅸ活性检测还可使用二期法和发色底物法。由于方法特性的不同,由某些特定基因突变位点导致的血友病A 患者其因子Ⅷ:C 一期法检测结果与临床出血表现不相符,可采用二期法和发色底物法进行测定。
6.5.5.3 5.5.3 待测血浆标本的稀释要求
应根据检测的凝血因子制定相应的血浆稀释倍数,目的是为了得到一个具有可接受斜率的曲线。因子Ⅷ和Ⅸ活性检测血浆标本至少应进行 2 个稀释度的检测,有条件的实验室可进行3 个稀释度的检测,对于低值标本可降低稀释倍数。
6.5.5.4 5.5.4 检测系统误差的来源
b) 使用曲线的平台区解释结果;
c) 不正确的孵育或活化时间;
d) 仪器操作方法不正确;
e) 仪器故障:如光源不稳定、温度波动、试剂溅出、试剂加入不准(量少)及电子干扰等;
f) 稀释不正确;
g) 冰冻血浆在-70℃条件下贮存超过 6 个月或者不适当的贮存环境;
h) 乏因子基质血浆含有>0.01 IU/mL(1%)的凝血活性,或含有凝血因子抑制物,或一个/多个凝血因子活性<50%。
6.5.6 5.6 室内质量控制
5.6.1 质控血浆的选择:实验室可使用商业质控血浆或自制质控血浆(冰冻血浆)进行室内质量控制,质控血浆应至少具有 2 个浓度水平(包含正常水平和异常水平),使用自制质控血浆时应与商业质控血浆进行同步检测以评价其适用性。实验室应根据实际工作需要确定质控血浆的数量,避免质控血浆批号更换过于频繁。
5.6.2 频率:实验室应根据检测标本量或检测批次确定室内质控的频率,并保证每次开机检测标本前至少进行一次正常水平和异常水平的室内质控;使用新开瓶/新复溶试剂进行标本检测前,宜首先进行质控品检测。
5.6.3 质控均值和允许范围的确定:每个批号质控血浆在使用前,应由实验室通过检测确定均值和允许范围,质控品制造商规定的“标准值”和“允许范围”只能作为参考。具体方法为:将质控血浆至少检测 10 d,每天至少检测 2 次,剔除超出 3SD 外数据,输入 20 次结果完成初始化,以20 次数据形成的均值作为当月质控图的中心线。SD、CV 在月末完成数据录入并确认后生成标值自动传递给下一月进行积累,这样每个月进行标值累积,直至累积达到指定月数(3~5 个月),计算累积均值和累积标准差,以此作为室内质控均值和标准差;室内质控建议选用 Westergard 质控规则,至少包括13s和22s规则,其余可根据实验室实际情况酌情选用。
5.6.4 实验室应记录结果并统计均值与标准差,绘制质控图。若发现结果失控应按步骤分析查找原因(检查试剂、质控血浆及仪器等),待各因素排查后再进行质控血浆的检测,质控结果在控后方可进行待测标本的检测。做好失控原因分析和采取的纠正措施记录。
5.6.5 实验室应定期(每月)统计室内质控结果,结果应符合 5.6.3 的要求。
6.5.7 5.7 室间质量评价
5.7.1 实验室应参加室间质量评价机构组织开展的室间质量评价活动,以保证采用相同实验室检测系统之间结果的可比性。
5.7.2 对于没有开展室间质评的项目应进行实验室间结果比对,以保证不同实验室之间结果的可比性。
6.5.8 5.8 检验结果的比对
若实验室内使用多个检测系统测定同一种分析物时,应定期进行结果比对(宜半年一次),至少使用20份临床标本(覆盖正常和低值标本)按照常规操作流程进行检测,正常浓度标本的比对偏倚应≤15%,低值浓度标本的比对偏倚应≤30%(或按照生产厂家和试剂介绍要求)。
6.6 6 检验后过程
6.6.1 6.1 参考区间
对于每个凝血因子,实验室可参照文献报道的参考区间进行验证后使用。若不适用,应根据所用仪器、试剂、采血方法、主要就医人群(成人或儿童)及所用抗凝剂建立适用于本室的参考区间。参考区间以相同的单位显示在每一份报告单上。
6.6.2 6.2 报告结果
报告前,应确定待测标本检测结果已乘以相应的稀释倍数,采用不同稀释比例测定值的平均值作为报告结果。报告单位为活性%或 IU/mL 均可,但需在检验报告中统一规范凝血因子活性报告单位及格式。超出定标曲线值以外的结果亦可报告以大于或小于相应的可读值报告,但应与临床联系,共同确定其原因。举例说明请见附录 B。
当怀疑凝血因子存在结构异常时,可考虑检测抗原,但抗原检测不是常规检测项目,多用于科研。
6.6.3 6.3 结果判读误差的来源
可能的结果判读误差来源包括(但不限于以下内容):
a) 未辨认出两条曲线缺乏平行;
b) 未辨认出两条曲线缺乏线性;
c) 采用推断的方法得到定标曲线范围之外的数据。
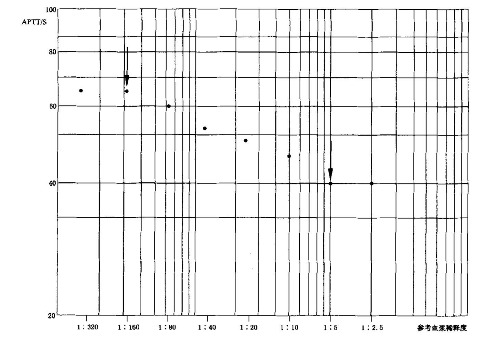
6.7 附录A(资料性)定标曲线手工绘制
采用手工法或部分半自动血液凝固分析仪进行检测时,需根据不同比例稀释标本的PT或APTT检测与对应的稀释比例在半对数或双对数坐标纸上手工绘制定标曲线,图应形成“S”型曲线,两端扁平,中间呈线性(图A.1,图A.2)。线性区计算所得r值应在 0.998~1.000、斜率应在0.9~1.1 范围内。

6.8 附录B(资料性)结果解读
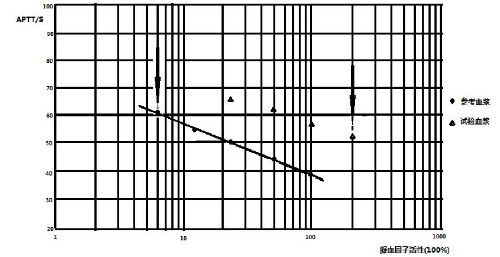
待测血浆标本经三点稀释后形成的标本结果曲线应形成一条与工作定标曲线平行的直线。若以上的情况不存在,应该考虑以下可能性:
a)若两个或更多邻近点形成一条平行于定标曲线的直线,但没有实验结果落在可读范围之内,进一步稀释参考血浆或受检血浆则可能产生可读结果(见图B.1);
b) 若仅一个试验结果落在可读范围,同时与邻近点形成的直线不平行于定标曲线,则应稀释受检血浆,以便获得可读结果;
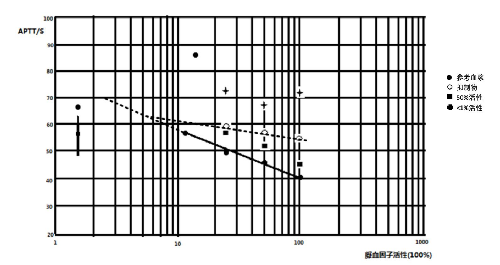
c) 若受检血浆与参考血浆曲线不呈平行,而一个以上的结果落在已知的线性范围内,则应当怀疑标本中有抑制物存在(见图B.2)。在报告结果时,以最高稀释度报告,同时应说明标本中可能有抑制物,应做有关检查确定;
d) 若所有的实验结果均落在线性范围之外,同时出现类似的试验结果(不考虑稀释所造成影响),这个现象提示所有的试验结果均位于“S”曲线的平台区。这是典型的严重凝血因子缺乏状态(见图B.2)。这种情况,应采用低值定标曲线进行测定,并且要求对标本进行两次测定。若患者血浆的凝固时间更延长,则患者结果可以低于该凝血因子检测最低限。
7 参考文献
[1] Determination of Coagulation Factor Activities Using the One-Stage ClottingAssay.2nd ed. CLSI guideline H48. Wayne PA: Clinical and Laboratory Standards Institute,2016
[2] Collection, Transport, and Processing of Blood Specimens for Testing Plasma-BasedCoagulation Assays and Molecular Hemostasis Assays. 5th ed. CLSI document H21-A5. WaynePA:Clinical and Laboratory Standards Institute, 2008
[3] WFH lab manual: 2000. Diagnosis of Haemophilia and Other Bleeding Disorders
[4] Joachim JP, Michael D, Andreas H. One-stage vs. chromogenic assays in haemophiliaA.European Journal of Haematology, 2014, 94 (Sup 77):38-44
[5] Kitchen S, Signer R.K, Key NS. Current laboratory practices in the diagnosisandmanagement of haemophilia: a global assessment. Haemophilia, 2015, 16:1-8
[6] Michael N, Lucas MB, Lorenzo A, et al. Variability between laboratories performingcoagulation tests with identical platforms: a nationwide evaluation study. Thromb J,2013,11(1):6
[7] Manuel DC. The diagnosis and management of congenital hemophilia. Semin ThrombHemost,2012, 38:727-734
[8] Jennings I, Kitchen DP, Woods TL, et al. Laboratory performance in the world federationof hemophilia EQA programme, 2003-2008. Haemophilia, 2009,15:571-577
[9] Fritsma GA, Dembitzer FR, Randhawa A, et al. Recommendations for appropriate activatedpartial thromboplastin time reagent selection and utilization. Am J Clin Pathol,2012,137:904-908
[10] Kitchen S, John DO, Preston FE. Quality in Laboratory Hemostasis and Thrombosis.Wiley-Blackwell, 2008
[11] Srivastava A, Santagostino E, Dougall A, et al. WFH guidelines for the managementof haemophilia, 3rd edition. Haemophilia, 2020, 26 (suppl 6):1-158
[12] User Evaluation of Between-Reagent lot variation; Approved Guideline. CLSI documentEP26-A. Wayne PA:Clinical and Laboratory Standards Institute, 2013
[13] Mackie I, Cooper P, Lawrie A, et al. Guidelines on the laboratory aspects ofassaysused in haemostasis and thrombosis. International Journal of Laboratory Hematology,2012,35(1):1-13