2 英文参考
Define and determine the reference intervals in clinical laboratory
《临床实验室检验项目参考区间的制定》由卫生部于2012年12月24日发布,自2013年8月1日起实施。
ICS 11.020
C 50
WS/T 402-2012
Define and determine the reference intervals in clinical laboratory
3 前言
本标准根据GB/T 1.1-2009给出的规则起草。
本标准由卫生部临床检验标准专业委员会提出。
本标准起草单位:第四军医大学西京医院、中国医科大学附属第一医院、复旦大学附属中山医院、北京大学第三医院、四川大学华西医院、广东省中医院、卫生部临床检验中心。
本标准主要起草人:郝晓柯、尚红、潘柏申、张捷、王兰兰、黄宪章、陈文祥、马越云、郑善銮、周铁成、彭道荣。
6 3 术语和定义
下列术语和定义适用于本文件。
3.1
参考个体 reference individual
按明确标准选择的用作检验对象的个体。
注:通常是符合特定标准的健康个体。
3.2
参考人群 reference population
由所有参考个体组成的群体。
注:通常参考人群中的个数是未知的,因此参考人群是一个假设实体。
3.3
参考样本组 reference sample group
从参考人群中选择的用以代表参考人群的足够数量的个体。
3.4
参考值 reference value
通过对参考个体某一特定量进行观察或者测量而得到的值(检验结果)。
3.5
参考分布 reference distribution
注:参考人群的分和分布参数可用参考样本组的分布和适宜的统计方法估计。
3.6
参考限 reference limit
注:参考限使规定部分的参考值分别小于等于或大于等于的下侧或上侧限值,参考限将参考值分类,参考限可能会与其他各种类型的医学决定限不同。
3.7
参考区间 reference range
两参考限之间(包括两参考限)的区间(参见附录A)。
注1:参考区间是指从参考下限到参考上限的区间.通常是中间95%区间。在某些情况下只有一个参考限具有临
床意义,通常是参考上限,这时的参考区间是0到参考上限。
7 4 参考个体选择
7.1 4.1 参考个体的筛选和分组
4.1.1 设计参考个体筛选标准
筛选参考个体时,应尽可能排除对结果有影响的因素,并设计详尽的调查表(参见附录B)以排除不符合要求的个体。针对不同的检验项目筛选标准不尽相同,主要考虑的因素有:
a) 饮酒情况(如酗酒);
b) 长期或近期献血;
c) 血压异常;
d) 近期与既往疾病;
g) 肥胖;
h) 吸毒;
i) 特殊职业;
j) 环境因素;
k) 饮食情况(如素食、节食等);
l) 近期外科手术;
m) 吸烟;
n) 遗传因素;
o) 输血史;
p) 滥用维生素;
q) 运动。
以上因素可用于筛选健康相关的参考个体,但需要注意两点:一是这些因素并不全面;二是不同的检验项目在筛选参考个体时,不一定要将上述指标全部纳入,筛选标准的增加或减少,要视其性质而定。
4.1.2 参考个体的分组
根据所筛选参考个体的特征进行分组。最常用的方式是按性别或年龄进行分组,下面列了一些可考虑的分组因素:
a) 年龄;
b) 性别;
c) 血型;
d) 种族;
e) 昼夜节律;
f) 取样时的状态及时问;
g) 月经周期;
h) 妊娠时期;
i) 锻炼(运动);
j) 饮食;
k) 吸烟;
l) 职业;
m) 其他。
7.2 4.2 参考个体选择
参考个体选择应保证研究对象的同质性,如调查季节、时间或空腹与否等。除4.1要求外,应接随机抽样方案选择参考个体。用于参考值检测的个体应尽可能涵盖各年龄组内不同年龄,不应集中在某一年龄段,应尽可能地接近使用该项目的临床患者的分布组成,男女个体数量相当,而且在地理区域选择上应具有代表性。除非是设计需要,否则不要选择住院或门诊病人。
8 5 参考样本分析前的准备
8.1 5.1 分析前准备内容
影响参考样本试验结果的因素有多种,包括分析前、分析中和分析后因素等。各种类型自动化分析仪的引进大大提高了临床分析的精密度,同时检测方法学的改进和校准品质量的提高,使得分析的准确度得到很大提高。但是分析前的影响因素常被临床医生和检验工作者所忽视。因此,应注意参考样本分析前的准备,主要有参考个体的状态、样本的数量、样本的采集,样本的处理与储存等几个方面。
8.2 5.2 参考个体的状态
参考个体的状态指对临床决策具有影响的状态。样本采集前是否空腹会对多种检验项目有直接或间接的影响,而长期节食也会造成许多指标的改变。另外,咖啡因、酒精、香烟和维生素C等也会影响许多分析物的性质,如改变一些酶类的活性。因此,应对照表1中列举的各因素进行参考个体。保证各种状态良好方可进行血液标本的检测。
表1 分析前的考虑因素

8.3 5.3 样本数量
5.3.1 以非参数方法估计样本的参考区间,至少需要120例,若需要分组则每组至少120人。若有离群值,则在剔除离群值后应补足。样本量最少为120是为了保证能正确估汁参考限的90%置信区间,若按99%置信区间估计,则最少需198例。
5.3.2 对于新生儿、幼儿、老年人等样本难以获得的人群,样本量可小于120例,但无论样本量为多少,均应采用非参数方法进行统计,并报告相应的百分位数。此外,还可以选用稳健法计算,该方法所需的最小样本量为20。
5.3.3 样本的分组,应在考虑临床实用性和是否符合生理要求的情况下,按照性别、年龄或其他因素进行。
8.4 5.4 样本采集
5.4.1 实验室应对样本的采集、处理和储存制定操作手册,有助于临床医师解读患者检测结果。
5.4.2 如果检测样本选择了血液,则应区分样本是动脉血、静脉血还是毛细管血,如需使用抗凝剂,应该使用哪种抗凝剂等。静脉血样本采集时应严格按照皮肤穿刺采集诊断血液样本的程序,应符合WS/T 225的规定。
5.4.3 若为其他体液样本如尿液、脑脊液或唾液等,也应规定相应的样本采集、加工和处理程序。
5.5 样本处理与储存
严格按照WS/T 225的规定进行。
9 6 参考值数据的检测、要求和分析
9.1 6.1 检测系统的要求
a) 参加室间质评,成绩合格。
c) 条件允许时,应对使用的检测系统进行精密度、正确度的验证。
e) 非配管系统应与配套系统进行比对试验,偏倚在允许的范围内。
f) 仪器操作步骤应严格按照生产厂商的要求或作业指导书进行,并准确无误地记录检测所得出的参考值数据。
9.2 6.2 参考值数据检测的要求和分析
6.2.1.1 在检测的数据中,如果有疑似离群的数据,应将疑似离群值的检测结果和其相邻值的差D和数据全距R相除,若D/R≥1/3考虑为离群值。
6.2.1.2 若有两个以上疑似离群值,可将最小的疑似离群值作如上处理,若都大于1/3,则需要将所有点都剔去;若都小于1/3,则保留所有数据。
6.2.1.3 剔除离群值后著样本量不足120例,则需补足。
6.2.2 绘制分布图
11 8 参考区间的验证
11.1 8.1 直接使用
分析厂家或其他实验室提供参考区间的原始资料,内容包括分析前、分析中和分析后程序,参考区间的估计方法,以及参考人群地理分布和人口统计学资料等。若实验室判断自己的情况与这些资料一致,则参考区间可不经验证直接使用。
11.2 8.2 小样本验证
若实验室希望或需要对参考区间进行验证,则实验室可以从本地参考人群中筛选少量参考个体(n= 20),将其测得值与参考区间的原始参考值相比较。需要注意的是:分析前和分析中因素应与参考区间提供实验室相一致。
按照筛选标准从本地参考人群中募集参考个体20人,采样并测定,测定值剔除离群值后若不满20例需补足。将这20个测定值与需验证的参考区间比较,若落在参考限外的测定值不超过2个,则该参考区间可直接使用;若3个或3个以上测定值超出,则需重新筛选20人,重复上述操作,同样若不超过2个测定值超出该参考区间的则可以使用,若仍然有3个或3个以上测定值超出,则实验室应重新检查所用的分析程序,考虑是否有人群差异,考虑是否需要自己建立参考区间。
11.3 8.3 大样本验证
对于某些重要项目的参考区间验证,实验室可以加大参考个体的样本量(n=60),将其测得值与参考区间的原始参考值相比较。同样,实验室的分析前和分析中因素应与提供参考区间的实验室一致。在统计学上,随着样本量的增加,利用统计原理发现实验室间人群差异的能力会更强。
按筛选标准得到参考个体,测定参考值,将其与需验证的参考区间比较,判断它们之间的差异是否显著。若没有显著性差异存在,则可以接受由制造商或其他实验室提供的参考区间;若有差异,一是实验室自己再增加参考个体的样本量达到IFCC制定参考区间最少样本量的要求,制定符合本地人群特征的参考区间;二是使用稳健法.直接利用这60名参考个体所提供的参考值计算参考区间。
不论是样本大小.若已知实验室所在地人群和参考区间原始人群之间在地理分布、人口统计学方面有差异,则没有必要验证,应考虑建立新的符合本地人群特征的参考区间。
12 9 参考区间确定
12.1 9.1 参考区间统计方法
9.1.1 正态分布统计
若数据呈正态分布,或检测数据经转换后亦呈正态分布,可按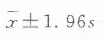
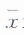
如,首先按统计学原理计算出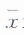
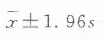
9.1.2 偏态分布统计
如果检测数据呈偏态分布,则可采用非参数法处理。将n个参考个体的观察值按从小到大的顺序排列,编上秩次:x1≤x2≤…≤xn。x1和xn分别为全部观察值的最小值和最大值。把这n个秩次分为100等分.与r%秩次相对应的数称为第r百分位数,以符号Pr表示。那么参考下限和参考上限的秩次可以分别用P2.5和P97.5表示,用r=0.025(n+1)和r=0.975(n+1)计算,若计算值不是整数,可将它们四舍五入后取整。
9.2 参考区间的分组
参考区间是否需要分组主要根据不同检验项目的临床意义。若需要则应作Z检验,以确定分组后的均值间有无统计上的显著性差异。
如,可将120个参考数据按分组要求分成两组(如:男、女或年龄两组),两个组的参考数据的个数较为接近。Z值计算见公式(1):

13 附录A(资料性附录)参考区间相关问题
13.1 A.1 参考区间描述
每一个定量的临床检测结果应与适当的参考区间相一致。在含有许多检测结果的报告中应包括检测这些参数的某种方法,而不只是参考区间。所确定的参考区间应反映亚组的区分,如性别、年龄等,尤其对于特殊群体,亚组的区分具有重要的意义。在报告中应使用术语“参考区间”,而不是使用“正常值”或“正常参考值”。
描述参考群体和参考区间应文件化,并存放在实验室操作者随手可得的地方。当实验室的某一个变化影响参考区间时,应随时更新文件,并详细记录参考区间变化的原因,包括参考群体的数量、统计学分析、健康标准的评估、参考样本的排除和区分标准以及分析使用的检测方法。
13.2 A.2 临界值(医学决定界限)
该文件不是描述“临界值”或其他医学决定限。医学决定限不同于参考区间,它是基于其他的科学和医学知识建立起来的。它与参考区间的得出方式是不同的,通常与某些特定的医学条件相关。
15 参考文献
[1] National Committee for Clinical Laboratory Standards. How to define,determine,and utilize reference intercals in the clinical laboratory;approved guideline. NCCLS Document C28-A. Wayne (PA):NCCLS;1995 June 59p.
[2] National Committee for Clinical Laboratory Standards. Interference testing in clinical chemistry. Proposed Guideline. NCCLS Document EP7-P. Wayne(PA):NCCLS;1986;
[3] Sizaret Ph,Anderson SG. The international reference preparation for alpha-fetoprotein.J Biol Standardization 1976;4:149.
