2 一、总则
生物检定法是利用生物体包括整体动物、离体组织、器官、细胞和微生物等评估药物生物活性的一种方法。它以药物的药理作用为基础,以生物统计为工具,运用特定的实验设计在一定条件下比较供试品和相当的标准品或对照品所产生的特定反应,通过等反应剂量间比例的运算或限值剂量引起的生物反应程度,从而测定供试品的效价、生物活性或杂质引起的毒性。
生物检定统计法主要叙述应用生物检定时必须注意的基本原则、一般要求、实验设计及统计方法。有关品种用生物检定的具体实验条件和要求,必须按照该品种生物检定法项下的规定。
2.1 生物检定标准品
凡中国药典规定用生物检定的品种都有它的生物检定标准品(S)。S都有标示效价,以效价单位 (u)表示,其含义和相应的国际标准品的效价单位一致。
2.2 供试品
供试品(T)或(U)是供检定其效价的样品,它的活性组分应与标准品基本相同。
AT或AU是T或U的标示量或估计效价。
2.3 等反应剂量对比
生物检定是将T和其S在相同的实验条件下同时对生物体或其离体器官组织等的作用进行比较,通过对比,计算出它们的等反应剂量比值(R),以测得T的效价PT。
R是S和T等反应剂量(dS、dT)的比值,即R=dS/dT。M是S和T的对数等反应剂量(xS、sT)之差,即M=lgdS-lgdT=xS-xT 。 R=antilgM。
PT是通过检定测得T的效价含量,称T的测得效价,是将效价比值(R)用T的标示量或估计效价AT校正之后而得,即PT=AT·R或PT=AT·antilgM。
检定时,S按标示效价计算剂量,T按标示量或估计效价(AT)计算剂量,注意调节T的剂量或调整其标示量或估计效价,使S和T的相应剂量组所致的反应程度相近。
2.4 生物变异的控制
生物检定具有一定的实验误差,其主要来源是生物变异性。因此生物检定必须注意控制生物变异,或减少生物变异本身,或用适宜的实验设计来减小生物变异对实验结果的影响,以减小实验误差。控制生物变异必须注意以下几点。
(1)生物来源、饲养或培养条件必须均一。
(2)对影响实验误差的条件和因子,在实验设计时应尽可能作为因级限制,将选取的因级随机分配至各组。例如体重、性别、窝别、双碟和给药次序等都是因子,不同体重是体重因子的级,雌性、雄性是性别因子的级,不同窝的动物是窝别因子的级,不同双碟是碟间因子的级,给药先后是次序因子的级等。按程度划分的级(如动物体重),在选级时,应选动物较多的邻近几级,不要间隔跳越选级。
(3)按实验设计类型的要求将限制的因级分组时,也必须严格遵守随机的原则。
2.5 误差项
指从实验结果的总变异中分去不同剂量及不同因级对变异的影响后,剩余的变异成分,用方差(S2)表示。对于因实验设计类型的限制无法分离的变异成分,或估计某种因级对变异的影响小,可不予分离者,都并入S2。但剂间变异必须分离。
不同的检定方法和实验设计类型,分别按有关的公式计算S2。
2.6 可靠性测验
平行线检定要求在实验所用的剂量范围内,对数剂量的反应(或反应的函数)呈直线关系,供试品和标准品的直线应平行。可靠性测验即验证供试品和标准品的对数剂量反应关系是否显著偏离平行偏离直线,对不是显著偏离平行偏离直线(在一定的概率水平下)的实验结果,认为可靠性成立,方可按有关公式计算供试品的效价和可信限。
2.7 可信限和可信限率
可信限(FL)标志检定结果的精密度。M的可信限是M的标准误SM和t值的乘积(t·SM),用95%的概率水平。M+t·SM是可信限的高限;M-t·SM是可信限的低限。用其反对数计算得R和PT的可信限低限及高限,是在95%的概率水平下从样品的检定结果估计其真实结果的所在范围。
R或PT的可信限率(FL%)是用R或PT的可信限计算而得。效价的可信限率为可信限的高限与低限之差除以2倍平均数(或效价)后的百分率。

计算可信限的t值是根据s2的自由度(f)查t值表而得。t值与f的关系见表一。
表一 t值表(P=0.95)
f | t |
3 4 5 6 7 8 9 10 11 12 | 3.18 2.78 2.57 2.45 2.37 2.31 2.26 2.23 2.20 2.18 |
f | t |
14 | 2.15 |
16 | 2.12 |
18 | 2.10 |
20 | 2.09 |
25 | 2.06 |
30 | 2.04 |
40 | 2.02 |
60 | 2.00 |
120 | 1.98 |
∞ | 1.96 |
各品种的检定方法项下都有其可信限率的规定,如果检定结果不符合规定,可缩小动物体重范围或年龄范围,或调整对供试品的估计效价或调节剂量,重复实验以减小可信限率。
对同批供试品重复试验所得n次实验结果(包括FL%超过规定的结果),可按实验结果的合并计算法算得PT的均值及其FL%作为检定结果。
3 二、直接测定法
直接测得药物对各个动物最小效量或最小致死量的检定方法。如洋地黄及其制剂的效价测定。
xS和xT为S和T组各只动物的对数最小致死量,它们的均值xS和xT为S和T的等反应剂量,nS和nT为S和T组的动物数。
3.1 1.效价计算
按(1)~(3)式计算M、R和PT。
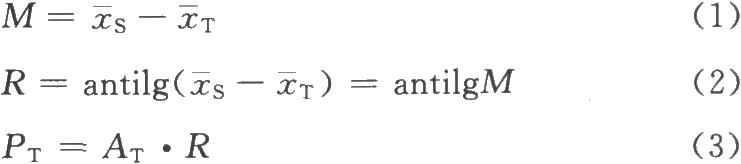
3.2 2.误差项及可信限计算
按(4)~(8)式计算s2、SM及R或PT的FL和FL%。
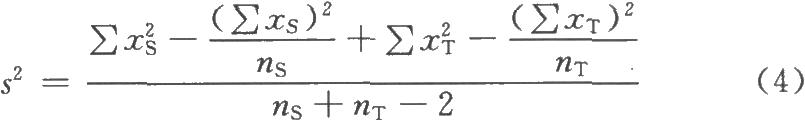
f=ns+nT-2,用此自由度查表一得t值。


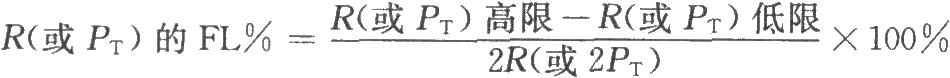 (8)
(8)
当两批以上供试品(T、U…)和标准品同时比较时,按(9)式计算S、T、U的合并方差S2。
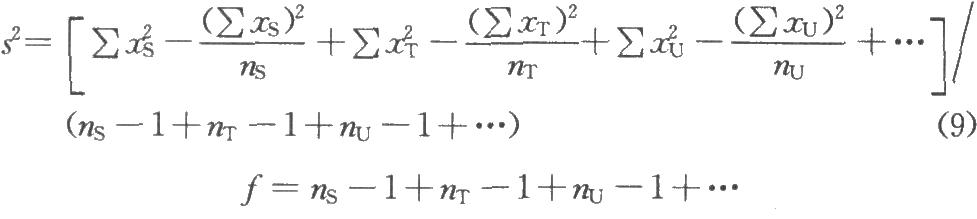
效价PT、PU…则是T、U分别与S比较,按(1)~(3)式计算。
例1 直接测定法
S为洋地黄标准品,按标示效价配成1.0u/ml的酊剂,临试验前稀释25倍。
T为洋地黄叶粉,估计效价AT=10u/g,配成1.0u/ml的酊剂,临试验前配成稀释液(1→25)。测定结果见表1-1。
S | T | ||
MLDs (dS) | xS | MLDT (dT) | xT |
u/kg体重 | lg(dS×10) | u/kg体重 | lg(dT×10) |
1.15 1.01 1.10 1.14 1.06 0.95 | 1.061 1.004 1.041 1.057 1.025 0.978 | 1.11 1.23 1.06 1.31 0.94 1.36 | 1.045 1.090 1.025 1.117 0.973 1.134 |
∑xs xS | 6.166 1.028 | ∑xT
| 6.384 1.064 |



4 三、量反应平行线测定法
药物对生物体所引起的反应随着药物剂量的增加产生的量变可以测量者,称量反应。量反应检定用平行线测定法,要求在一定剂量范围内,S和T的对数剂量x和反应或反应的特定函数y呈直线关系,当S和T的活性组分基本相同时,两直线平行。本版药典量反应检定主要用(2.2)法、(3.3)法或(2.2.2)法、(3.3.3)法,即S、T(或U)各用2个剂量组或3个剂量组,统称(k·k)法或(k·k·k)法;如果S和T的剂量组数不相等,则称(k·k')法;前面的k代表S的剂量组数,后面的k或k’代表T的剂量组数。一般都是按(k·k)法实验设计,当S或T的端剂量所致的反应未达阈值,或趋于极限,去除此端剂量后,对数剂量和反应的直线关系成立,这就形成了(k·k')法。例如(3.3)法设计就可能形成(2.3)法或(3.2)法等。因此,(k·k')法中的k只可能比k'多一组或少一组剂量。(k·k')法的计算结果可供重复试验时调节剂量或调整供试品估计效价时参考。无论是(k·k)法、(k·k')法或(k·k·k)法,都以K代表S和T的剂量组数之和,故K=k+k或K=k+k'或K=k+k+k。
本版药典平行线测定法的计算都用简算法,因此对各种(k·k)法要求:
(1)S和T相邻高低剂量组的比值(r)要相等,一般r用(1:0.8)~(1:0.5),lgr=I。
4.1 1.平行线测定的实验设计类型
根据不同的检定方法可加以限制的因级数采用不同的实验设计类型。本版药典主要用下面三种实验设计类型。
4.1.1 (1)随机设计
剂量组内不加因级限制,有关因子的各级随机分配到各剂量组。本设计类型的实验结果只能分离不同剂量(剂间)所致变异,如绒促性素的生物检定。
4.1.2 (2)随机区组设计
将实验动物或实验对象分成区组,一个区组可以是一窝动物、一只双碟或一次实验。在剂量组内的各行间加以区组间(如窝间、碟间、实验次序间)的因级限制。随机区组设计要求每一区组的容量(如每一窝动物的受试动物只数、每一只双碟能容纳的小杯数等)必须和剂量组数相同,这样可以使每一窝动物或每一只双碟都能接受到各个不同的剂量。因此随机区组设计除了从总变异中分离剂间变异之外,还可以分离区组间变异,减小实验误差。例如抗生素杯碟法效价测定。
4.1.3 (3)交叉设计
同一动物可以分两次进行实验者适合用交叉设计。交叉设计是将动物分组,每组可以是一只动物,也可以是几只动物,但各组的动物只数应相等。标准品(S)和供试品(T)对比时,一组动物在第一次试验时接受S的一个剂量,第二次试验时则接受T的一个剂量,如此调换交叉进行,可以在同一动物身上进行不同试品、不同剂量的比较,以去除动物闻差异对实验误差的影响,提高实验精确度,节约实验动物。(2.2)法S和T各两组剂量,用双交叉设计,将动物分成四组;对各组中的每一只动物都标上识别号。每一只动物都按给药次序表进行两次实验。
双交叉设计两次实验的给药次序表
第一组 | 第二组 | 第三组 | 第四组 | |
第一次实验 第二次实验 | dS1 dT2 | dS2 dT1 | dT1 dS2 | dT2 dS1 |
4.2 2.平行线测定法的方差分析和可靠性测验
(l)将反应值或其规定的函数(y)按S和T的剂量分组列成方阵表见表二。
表二 剂量分组方阵表
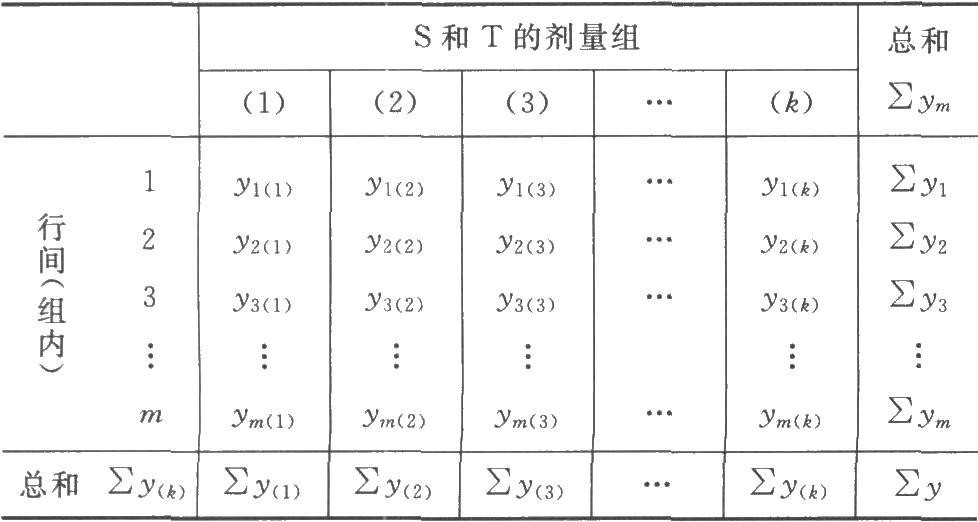
方阵中,K为S和T的剂量组数和,m为各剂量组内y的个数,如为随机区组设计,m为行间或组内所加的因级限制;n为反应的总个数,n=mK。
(2)特异反应剔除和缺项补足
特异反应剔除 在同一剂量组内的各个反应中,如出现个别特大或特小的反应,应按下法判断其是否可以剔除。
设ya表示特异反应值(或其规定的函数),ym为与ya相对的另一极端的反应值,y2、y3为与ya最接近的两个反应值,ym-1、ym-2为与ym最接近的两个反应值,m是该剂量组内的反应个数,将各数值按大小次序排列如下:
ya、y2、y3…ym-2、ym-1、ym
如ya为特大值,则依次递减,ym最小;如ya为特小值,则依次递升,ym最大。按(10)~(12)式计算J值。
当m=3~7时

当m=8~13时

当m=14~20时

如,的计算值大于J值表(表三)中规定的相应数值时,ya即可剔除。
表三 剔除特异反应的J值表
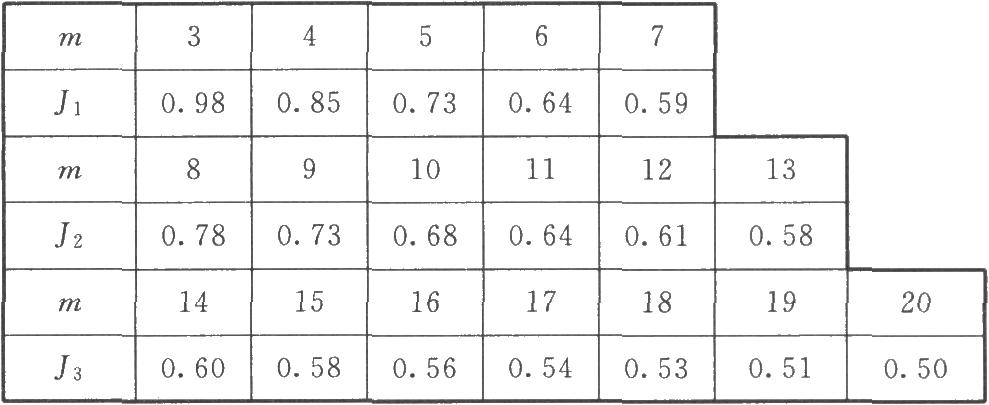
缺项补足 因反应值被剔除或因故反应值缺失造成缺项,致m不等时,根据实验设计类型做缺项补足,使各剂量组的反应个数m相等。
随机设计 对缺失数据的剂量组,以该组的反应均值补入,缺1个反应补1个均值,缺2个反应补2个均值。
随机区组设计 按(13)式计算,补足缺项。

如果缺1项以上,可以分别以y1、y2、y3等代表各缺项,然后在计算其中之一时,把其他缺项y直接用符号y1、y2等当作未缺项代人(13)式,这样可得与缺项数相同的方程组,解方程组即得。
随机区组设计,当剂量组内安排的区组数较多时,也可将缺项所在的整个区组除去。
随机设计的实验结果中,如在个别剂量组多出1~2个反应值,可按严格的随机原则去除,使各剂量组的反应个数m相等。
不论哪种实验设计,每补足一个缺项,就需把s2的自由度减去1,缺项不得超过反应总个数的5%。
(3)方差分析 方阵表(表二)的实验结果,按(14)~(21)式计算各项变异的差方和、自由度(f)及误差项的方差(s2)。
随机设计 按(14)式、(15)式计算差方和(总)、差方和(剂间)。按(20)式计算差方和(误差)。按(18)式或(21)式计算s2。
随机区组设计 按(14)~(17)式计算差方和(总)、差方和(剂间)、差方和(区组间)、差方和(误差)。按(18)式或(19)式计算s2。

f(总)=mK-1


(4)可靠性测验 通过对剂间变异的分析,以测验S和T的对数剂量和反应的关系是否显著偏离平行直线。(2.2)法和(2.2.2)法的剂间变异分析为试品间、回归、偏离平行三项,其他(k·k)法还需再分析二次曲线、反向二次曲线等。
(k·k)法、(k·k')法按表四计算各变异项的m·∑C2i及∑[Ci·∑y(k)],按(22)式计算各项变异的差方和。
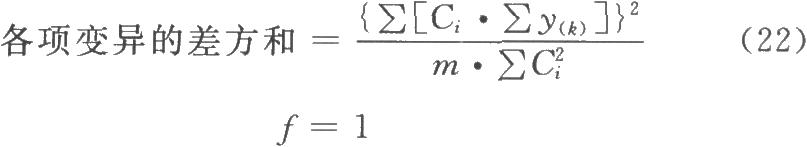
表四 (k·k)法、(k·k')法可靠性测验正交多项系数表(k·k·k)法按(23)式、(24)式计算试品间差方和。
(2.2.2)法
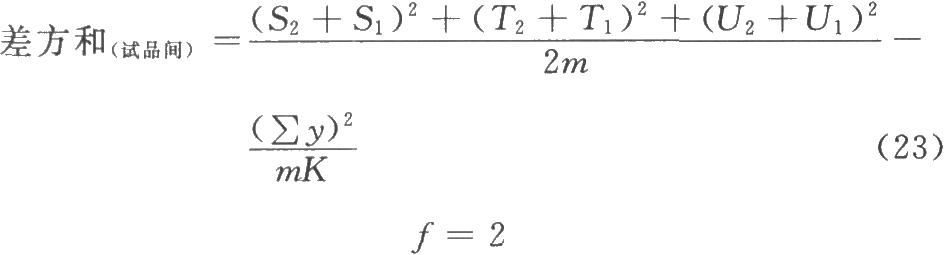
(3.3.3)法

按表五计算回归、二次曲线、反向二次曲线各项变异的m·∑C2i及∑[Ci·∑y(k)];按(22)式计算差方和(回归)、差方和(二次曲线)。
表五 (k·k·k)法可靠性测验正交多项系数表
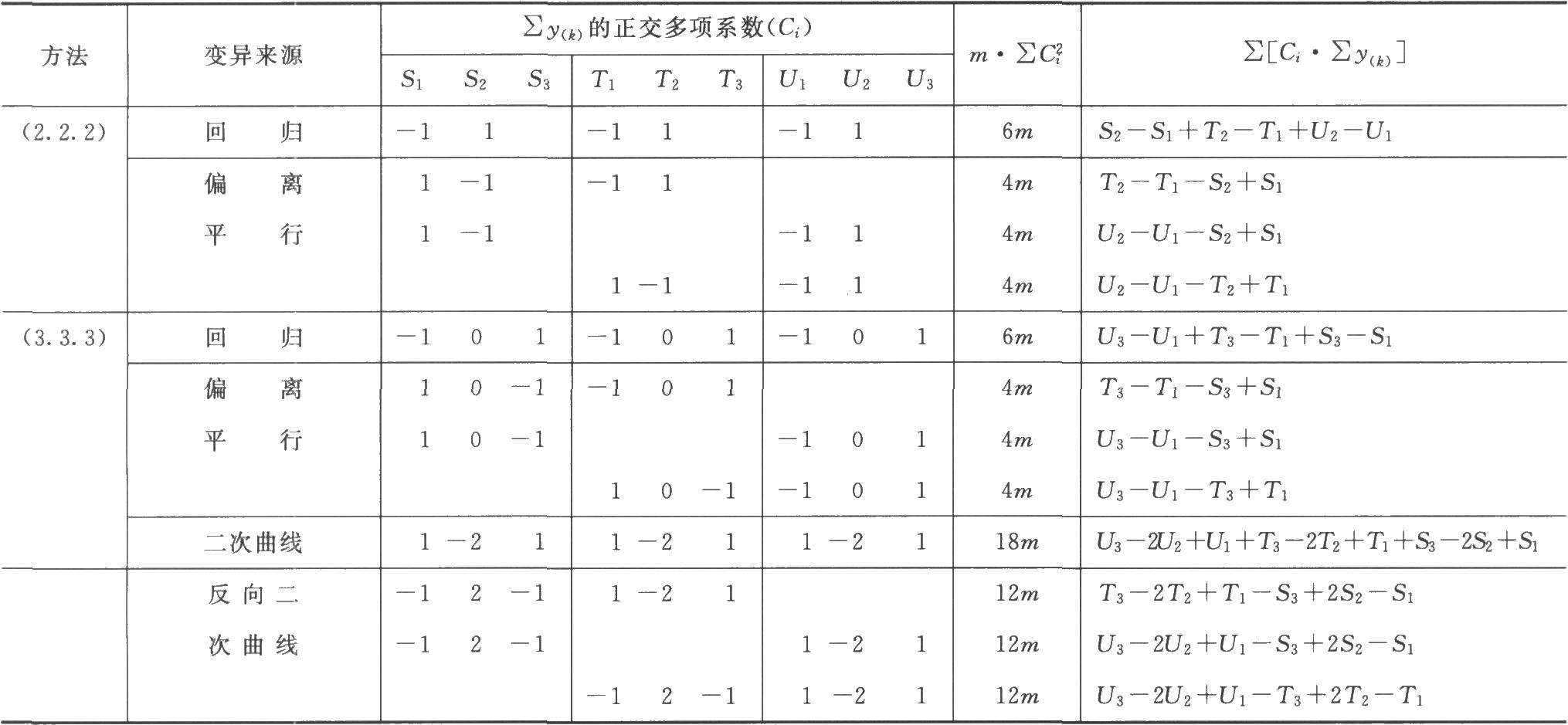
按(25)式计算差方和(偏离平行)及差方和(反向二次曲线)。

将方差分析结果列表进行可靠性测验。例如随机区组设计(3.3)法可靠性测验结果列表,见表六。
裹六 随机区组设计(3.3)法可靠性测验结果
变异来源 | f | 差方和 | F | P | |
试品间 回归 偏离平行 二次曲线 反向二次曲线 | 1 1 1 1 1 | (22)式 (22)式 (22)式 (22)式 (22)式 | 差方和/f 差方和/f 差方和/f 差方和/f 差方和/f | 方差/S2 方差/S2 方差/S2 方差/S2 方差/S2 | |
剂间 区组间 | K-1 m-1 (K-1)(m-1) | (15)式 (16)式 (17)式 | 差方和/f 差方和/f 差方和/f(s2) | 方差/S2 方差/S2 | |
总 | mK-l | (14)式 |
表六中概率P是以该变异项的自由度为分子,误差项(S2)的自由度为分母,查F值表(表七),将查表所得F值与表六F项下的计算值比较而得。当F计算值大于P=0.05或P=0.01的查表值时,则P<0.05或P<0.01,即为在此概率水平下该项变异有显著意义。
可靠性测验结果,回归项应非常显著(P<0.01)。(2.2)法、(2.2.2)法偏离平行应不显著(P>0.05)。其他(k·k)法、(k·k·k)法偏离平行、二次曲线、反向二次曲线各项均应不显著(P>0.05)。
试品间一项不作为可靠性测验的判断标准,试品间变异非常显著者,重复试验时,应参考所得结果重新估计T的效价或重新调整剂量试验。
双交叉设计的方差分析和可靠性测验
(1)双交叉设计实验结果的方阵表 将动物按体重随机分成四组,各组的动物数(m)相等,四组的动物总数为4m。对四组中的每一只动物都加以识别标记,按双交叉设计给药次序表进行实验,各组的每一只动物都给药两次,共得2×4m个反应值。将S、T各两个剂量组两次实验所得反应值排列成表,见表八。
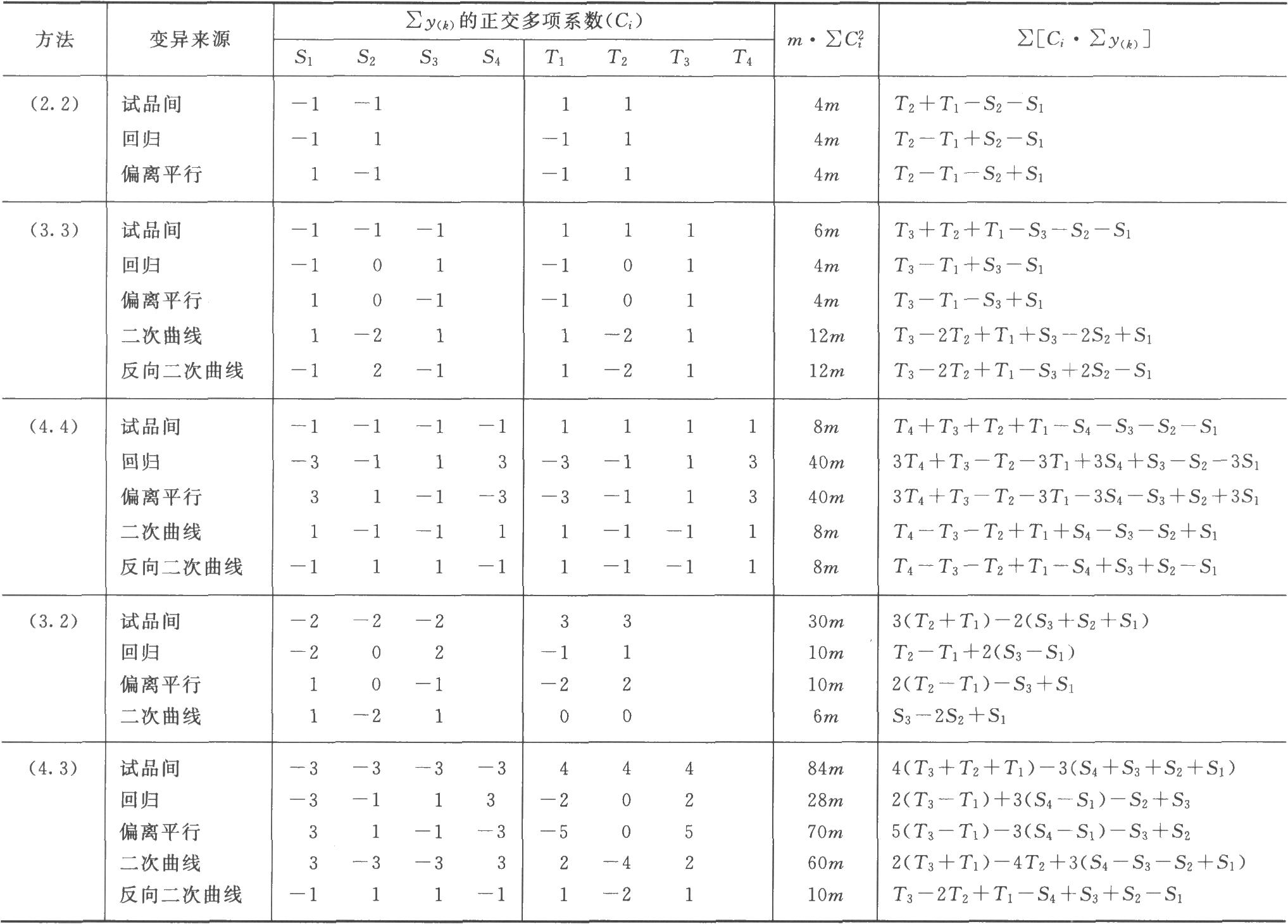
注:用(2.3)法及(3.4)法时,分别将(3.2)法及(4.3)法中S和T的正交多项系数互换即得。
表中S1、S2、T1、T2…在量反应分别为标准品和供试品每一剂量组内的反应值或它们规定函数的总和[相当于表二的∑y(k)各项]。所有足序1、2、3……都是顺次由小剂量到大剂量,Ci是与之相应的正交多项系数。m·∑C2i是该项变异各正交多项系数的平方之和与m的乘积,∑[Ci·∑y(k)]为S1、S2…T1、T2…分别与该项正交多项系数乘积之和。
表七 F值表

注:上行,P=0.05;下行,P=0.01。
表八 双交叉实验结果
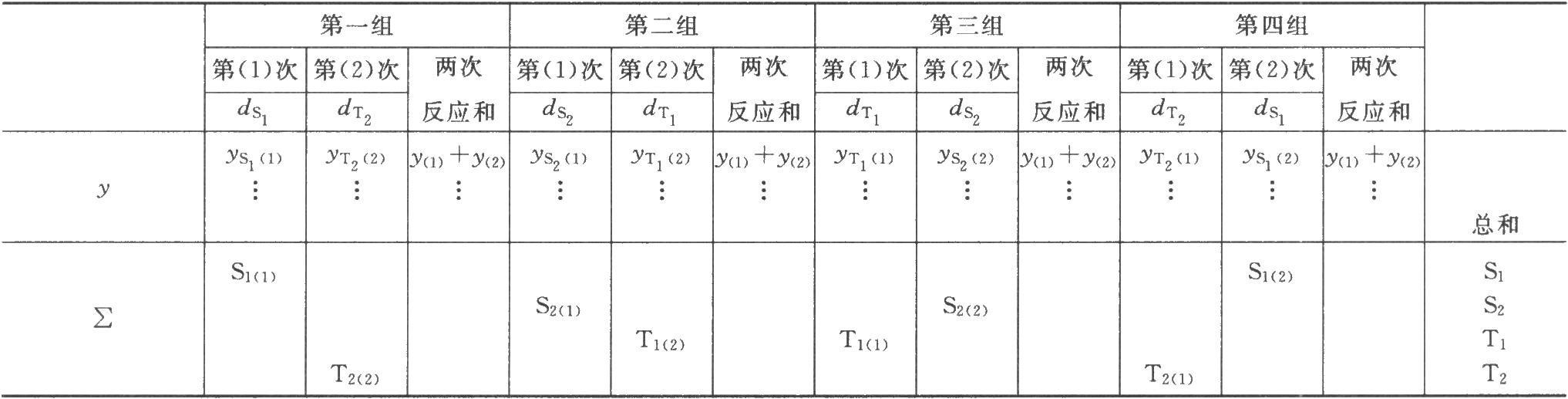
(2)缺项补足 表八中如有个别组的1个反应值因故缺失,均作该只动物缺失处理,在组内形成两个缺项。此时,可分别用两次实验中该组动物其余各反应值的均值补入;也可在其余三组内用严格随机的方法各去除1只动物,使各组的动物数相等。每补足一个缺项,误差(Ⅰ)和误差(Ⅱ)的方差s2Ⅰ和s2Ⅱ的自由度都要减去1。缺项不得超过反应总个数的
5%。同一组内缺失的动物不得超过1只。
(3)方差分析 双交叉设计的总变异中,包含有动物间变异和动物内变异。对表八的2×4m个反应值进行方差分析时,总变异的差方和(总)按(26)式计算。
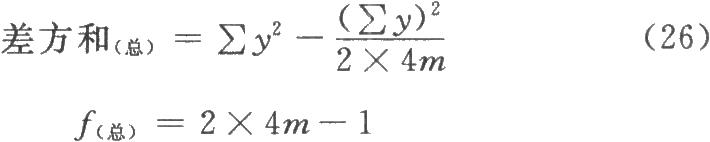
动物间变异是每一只动物两次实验所得反应值的和(表八每组动物的第三列)之间的变异,其差方和按(27)式计算。

动物间变异和动物内变异的分析 将表八中S和T各剂量组第(1)次实验所得反应值之和S1(1)、S2(1)、T1(1)、T2(1)及第(2)次实验反应值之和S1(2)、S2(2)、T1(2)、T2(2)按表九双交叉设计正交系数表计算各项变异的m·∑C2i及∑(Ci·y),按(22)式计算各项变异的差方和。
总变异的差方和减去动物间变异的差方和,再减去动物内各项变异的差方和,余项为误差(Ⅰ)的差方和,按(28)式计算。

误差(I)的方差s2,用以计算实验误差SM、FL,及进行动物内各项变异(表九中*标记者)的F测验。
误差(Ⅱ)的差方和为动物间变异的差方和减去表九中其余三项变异(表九中无*标记者)的差方和,按(29)式计算。
表九 双交叉设计正交系数表①
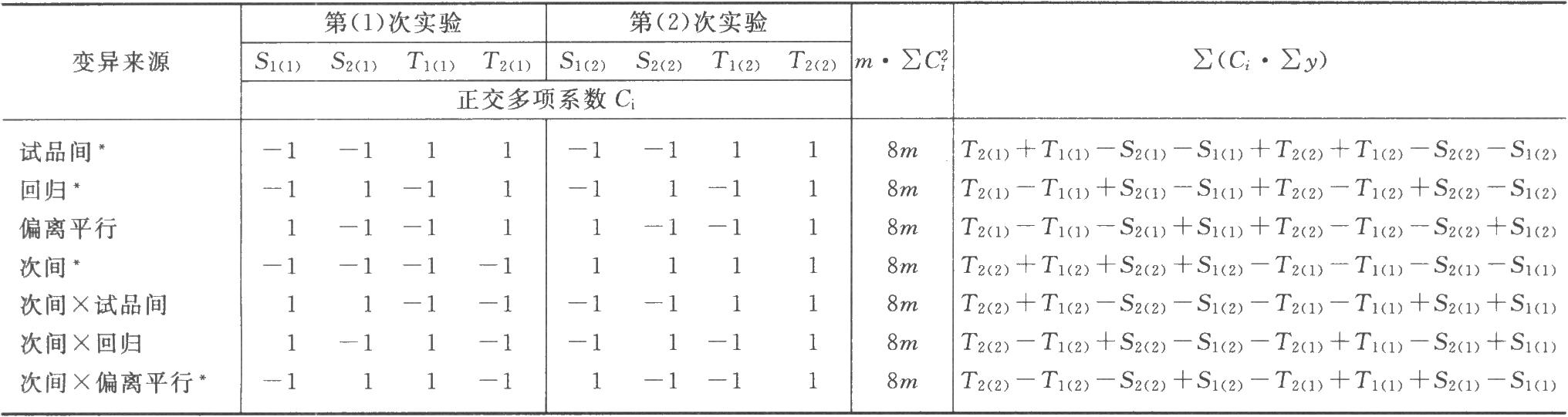
①各项变异的自由度均为1。有*号标记的四项为动物内变异,其余三项为动物间变异。

(4)可靠性测验 将方差分析及F测验的结果列表,如表十。
表十中的概率P,计算同表六,但表的上半部分是以s2Ⅱ的自由度为分母,表的下半部分以s2的自由度为分母,查F值表(表七),将查表所得的F值与表十F项下的计算值比较而得。
表十 双交叉设计可靠性测验结果

可靠性测验结果判断 回归、偏离平行、试品间三项的判断标准同(2.2)法。
次间×试品间、次间×回归、次间×偏离平行三项中,如有F测验非常显著者,说明该项变异在第一次和第二次实验的结果有非常显著的差别,对出现这种情况的检定结果,下结论时应慎重,最好复试。
4.3 3.效价(PT)及可信限(FL)计算
各种(k·k)法都按表十一计算V、W、D、A、B、g等数值,代入(30)~(33)式及(3)式、(8)式计算R、PT、SM以及R、PT的FL和FL%等。
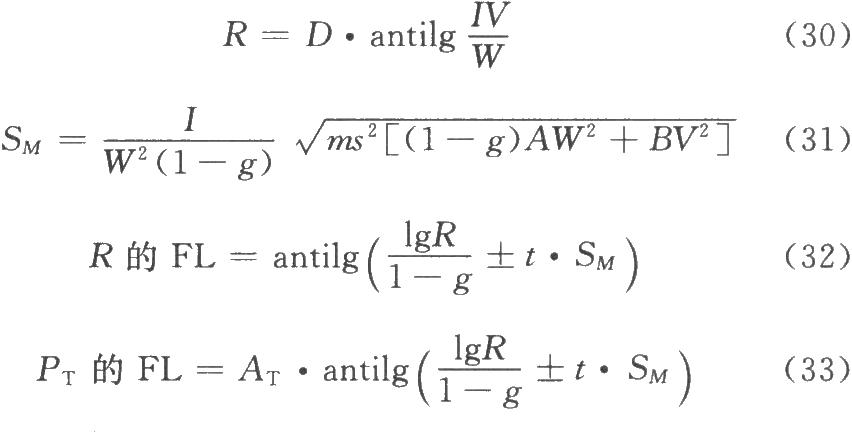
(2.2)法双交叉设计 计算方法同上述(2.2)法。双交叉设计各剂量组都进行两次试验,S和T每一剂量组的反应值个数为组内动物数的两倍(2m)。
(1)双交叉设计用S和T各组剂量两次试验所得各反应值之和(表八中的S1、S2、T1、T2)按表十一(2.2)法公式计算V、W、D、g等数值。
表十一 量反应平行线检定法的计算公式①
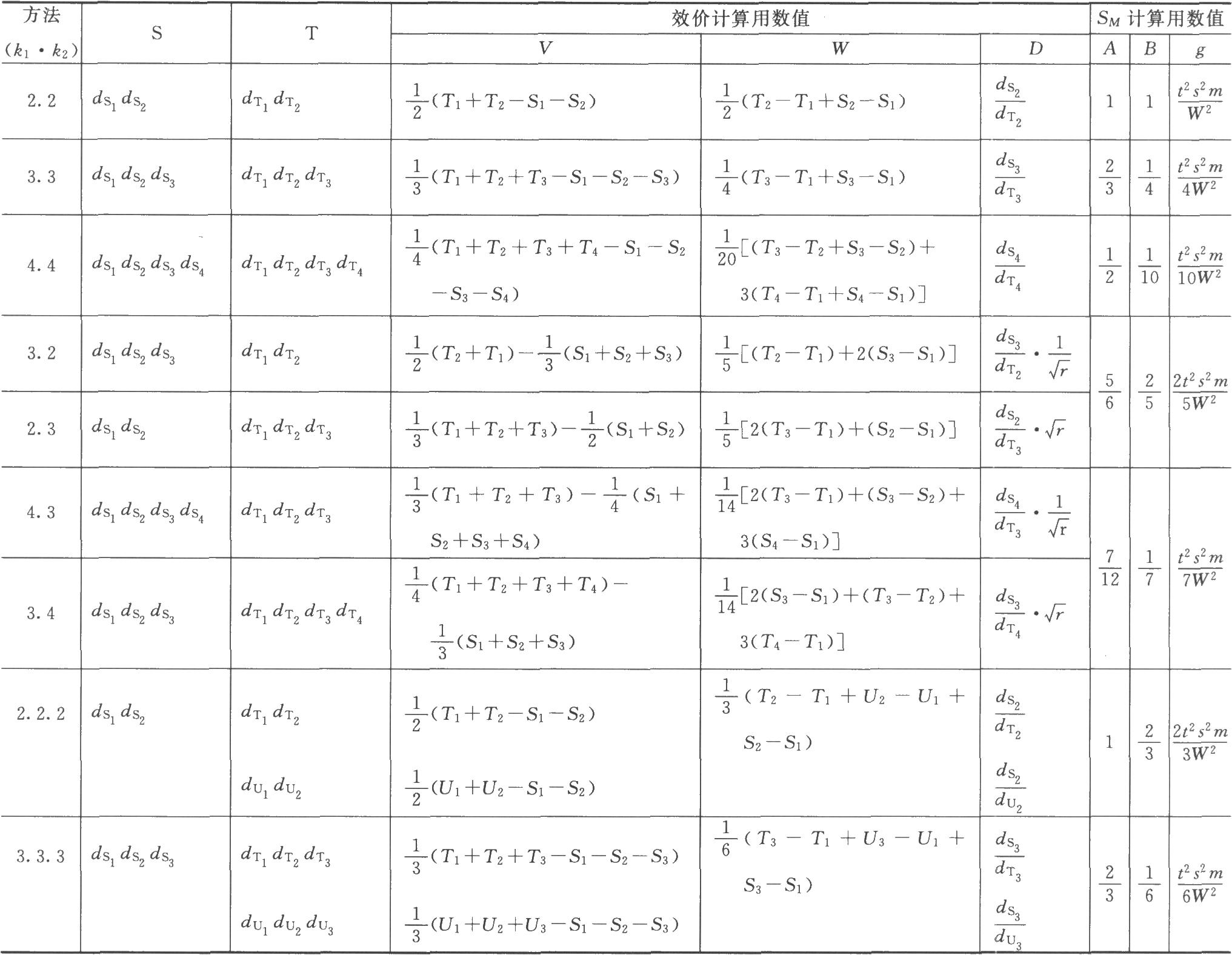
①表中dS、dT分别为S和T的剂量,下角1、2、3是顺次由小剂量到大剂量。
(2)参照(31)式计算SM,因每只动物进行两次实验,式中m用2m代替,(2.2)法A=1,B=1,SM的公式为
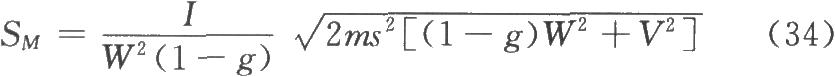
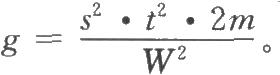
例2 量反应平行线测定随机设计(3.3.3)法绒促性素(HCG)效价测定——小鼠子宫增重法

表2-1 HCG效价测定结果
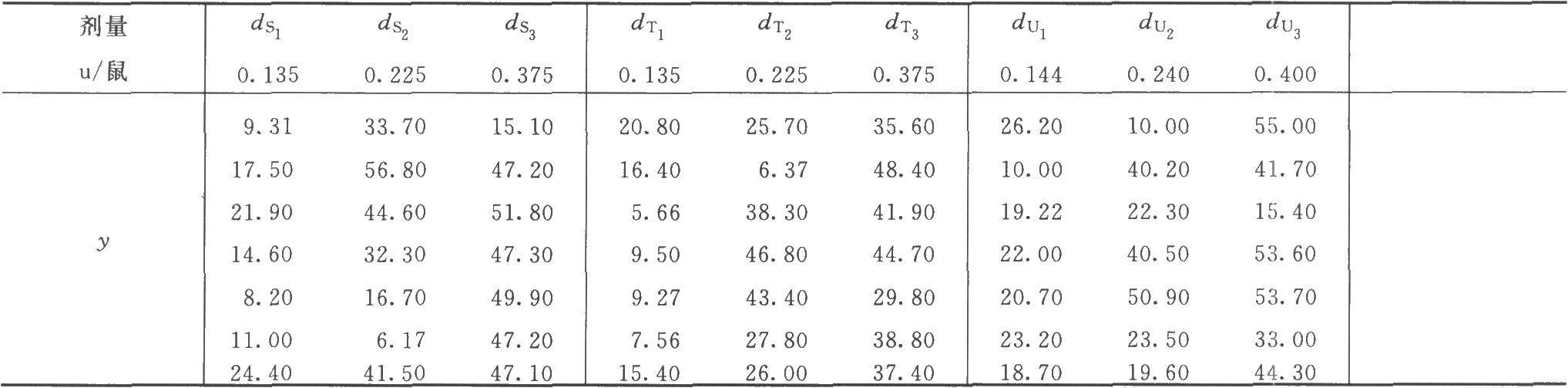
续表

(3.3.3)法,K=9;每组15只小鼠,m=15
(1)按(14)式、(15)式、(20)式计算各项的差方和

(2)剂间变异分析及可靠性测验 按(24)式及表五 (3.3.3)法分析。

各项分析结果见表2-2、表2-3。
结论:回归非常显著,偏离平行、二次曲线、反向二次曲线均不显著,实验结果成立。
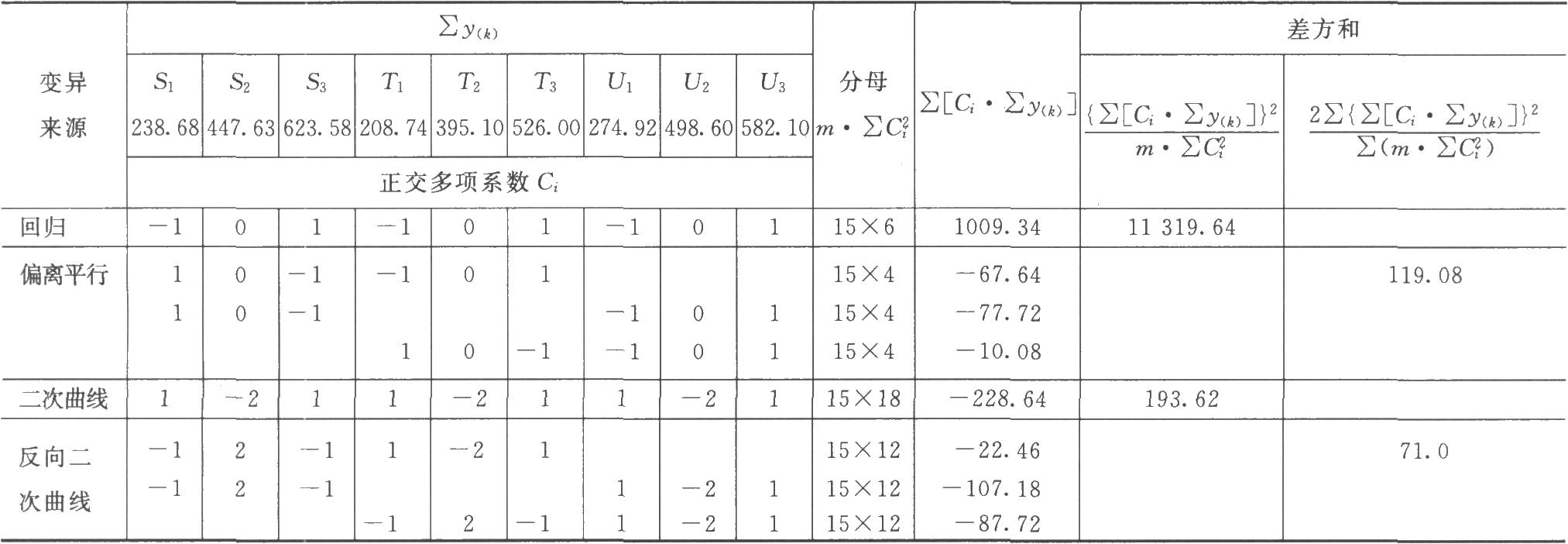
表2-3 HCG效价测定(3.3.3)法可靠性测验结果

(3)效价(PT、PU)及可信限(FL)计算 按表十一(3.3.3)法及(30)~(33)式、(3)式、(8)式计算。


例3 量反应平行线测定随机区组设计(3.3)法新霉素效价测定——杯碟法
稀释液dS1:8.0u/ml ds2:10.:0u/ml ds3:12.5u/ml
T为新霉素 标示量 AT:670u/mg
稀释液dT:8.0u/ml
dT2:10.0u/ml
dT3:12.5 u/ml
r=1:0.8
I=0.0969
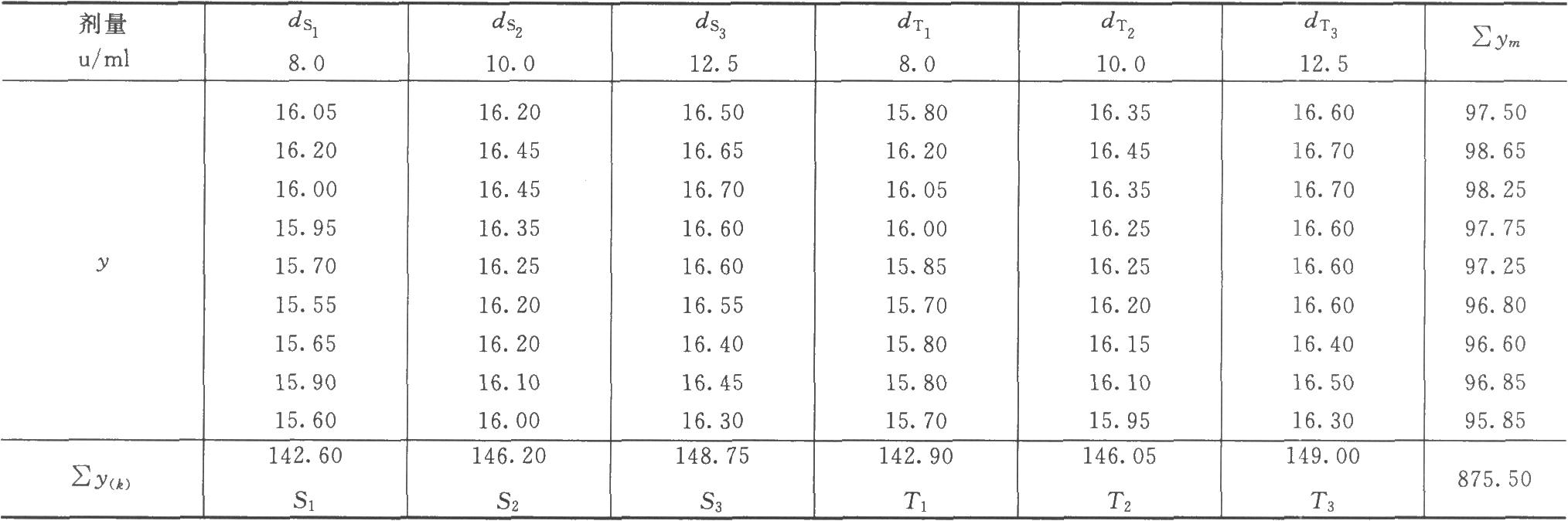
随机区组设计(3.3)法,K=6
不同双碟(碟间)是剂量组内所加的因级限制,共9个双碟,m=9。
(1)按(14)~(18)式计算各项差方和


(2)剂间变异分析及可靠性测验 按表四(3.3)法计算,结果见表3-2、表3-3。
结论:回归非常显著(P<0.01),偏离平行、二次曲线、反向二次曲线均不显著(P>0.05),实验结果成立。组内(碟间)差异非常显著(P<0.01),分离碟间差异,可以减小实验误差。
(3)效价(PT)及可信限(FL)计算 按表十一(3.3)法及(30)~(33)式、(3)式、(8)式计算。

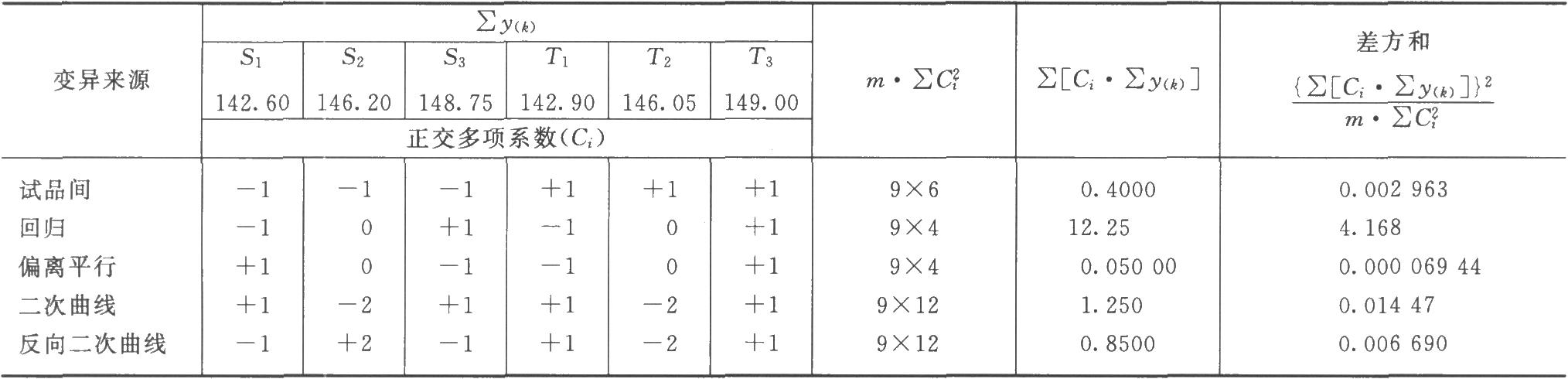
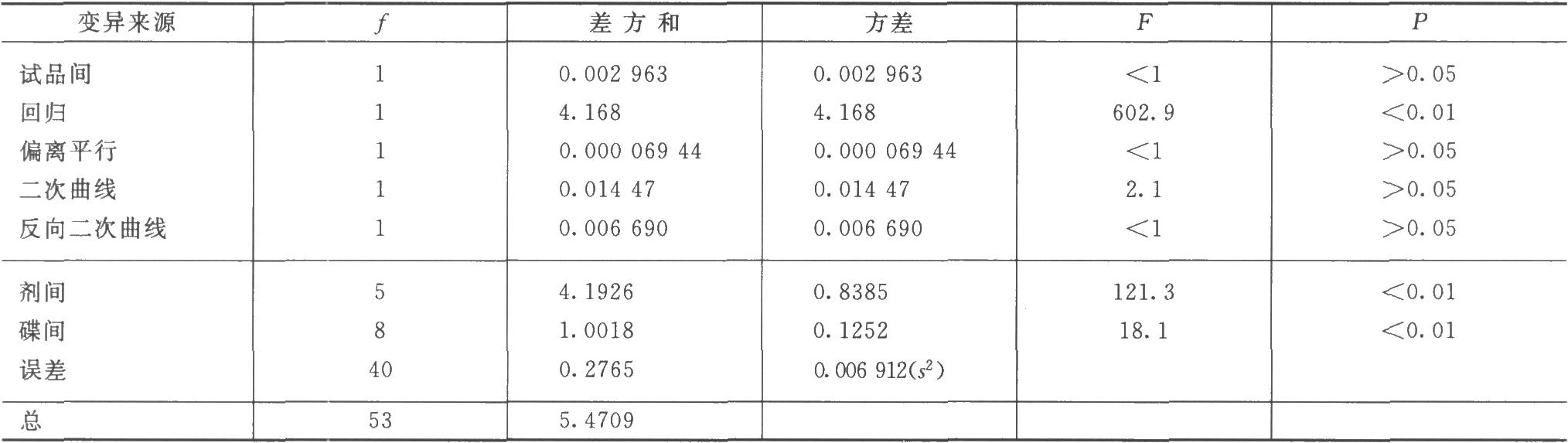


和表3-3结果相同。
例4 量反应平行线测定随机区组设计(2.2)法缩宫素效价测定——大鼠离体子宫法
dS1:0.0068u dS2:0.009u
T为缩宫素注射液 标示量AT:10u/ml
dT1:0.008u dT2:0.0106u
r=1:0.75 I=0.125
随机区组设计(2.2)法,K=4。每组4个剂量为一区组,其给药次序为剂量组内所加因级限制。各剂量组均为5个反应,m=5。

(1)特异反应处理 表4-1第三列第四行dT,的第4个数值特小,本例为随机区组设计按(10)式计算决定此值是否属特异值。
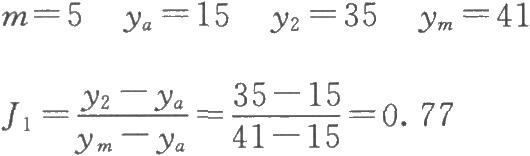
查表三,m=5时,J1=0.73,小于计算值0.77,故此值可以剔除。剔除后形成的缺项按(13)式补足。

(2)按(14)~(18)式计算各项差方和 补足了一个缺项,误差项的自由度按(17)式再减1。

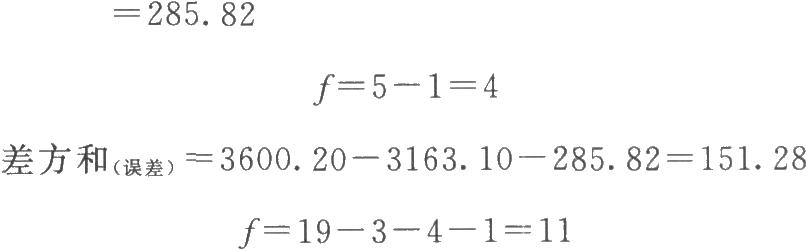
(3)剂间变异分析及可靠性测验 按表四(2.2)法计算,结果见表4-2、表4-3。
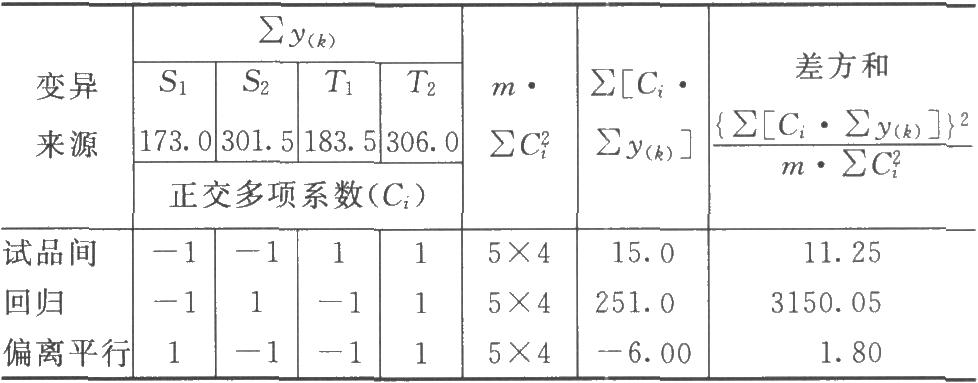

结论:回归非常显著(P<0.01),偏离平行不显著(P>0.05),实验结果成立。
区组间差异显著(P<0.05),分离区组间变异,可以减小实验误差。
缩宫素离体子宫效价测定,如区组间变异不显著,也可以不分离区组间变异,用随机设计方差分析法计算。
(4)效价(PT)及可信限(FL)计算 按表十一(2.2)法及(30)~(33)式、(3)式、(8)式计算。

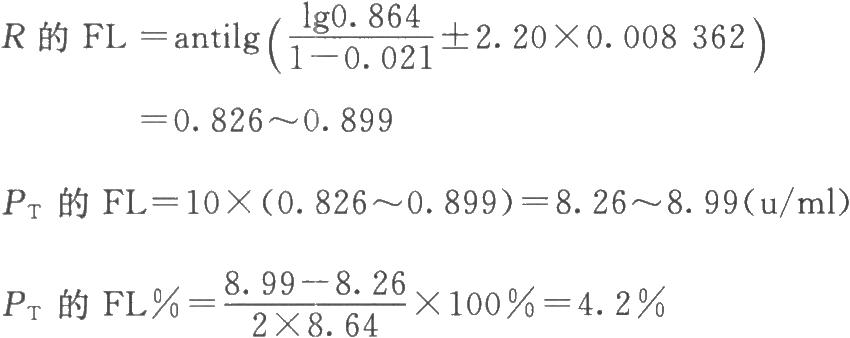
例5 量反应平行线测定(2.2)法双交叉设计胰岛素效价测定——小鼠血糖法


(1)方差分析 按(26)式、(27)式计算:

f(动物间)=4×10-1=39
(2)将表5-1中S、T各剂量组每一次反应值之和按表九及(22)式、(28)式、(29)式、(18)式计算各项变异的m·∑C2i、∑(Ci·∑y)及差方和、方差,并进行可靠性测验,结果见表5-2、表5-3。按(28)式、(29)式计算:

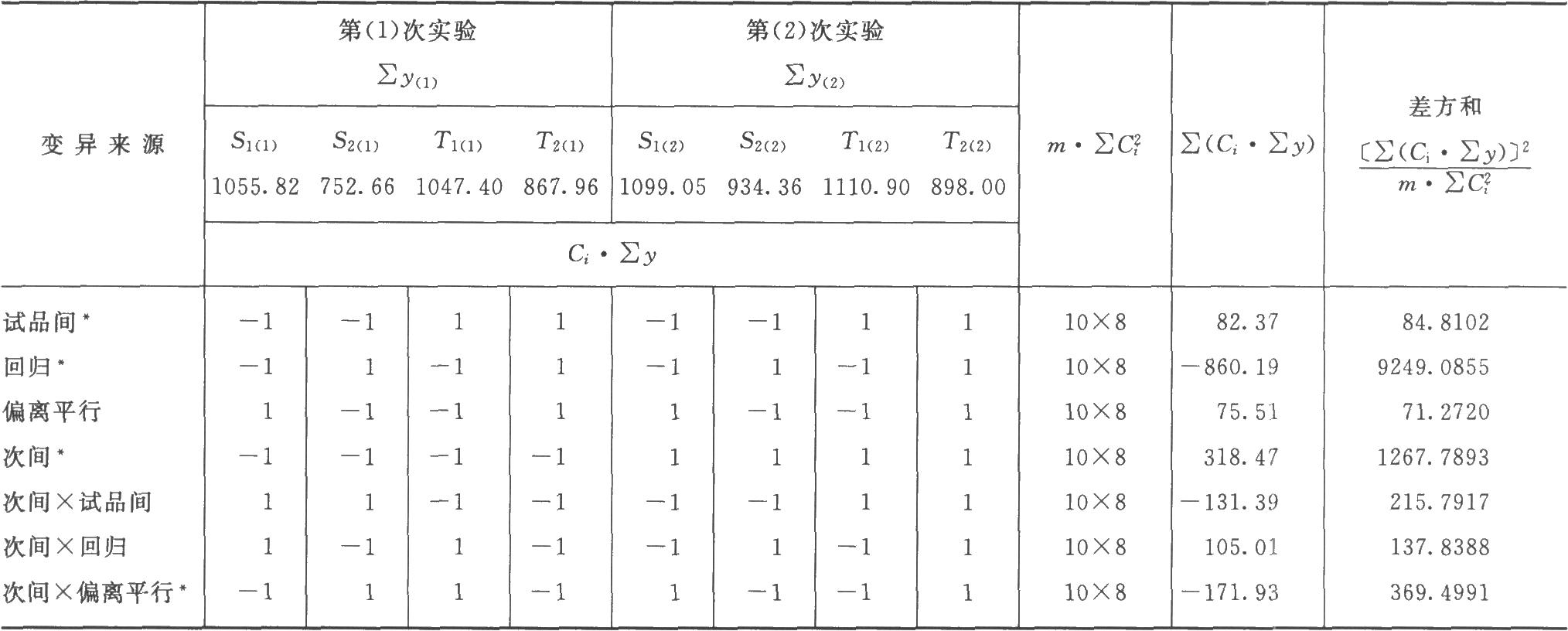
表5-3 胰岛素双交叉法可靠性测验结果

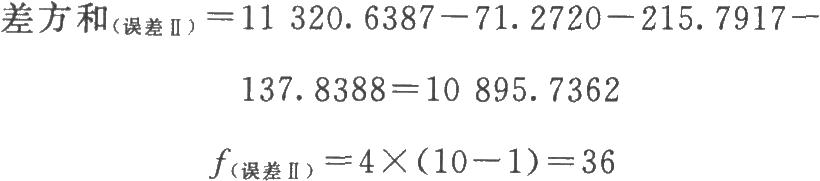
结论:回归非常显著,偏离平行不显著,实验结果成立。两次实验间的差异非常显著,用双交叉设计可以消除实验间变异对实验误差的影响,提高实验的精确度。
(3)效价(PT)及可信限(FL)计算:
用表5-1的S1、S2、T1、T2,按表十一(2.2)法及(30)式、(32)~(34)式等计算:


四、实验结果的合并计算
同一批供试品重复n次测定,所得n个测定结果,可用合并计算的方法求其效价PT的均值及其FL。
参加合并计算的n个结果应该是:
(1)各个实验结果是独立的,完整的,是在动物来源、实验条件相同的情况下,与标准品同时比较所得的检定结果(PT)。
(2)各次检定结果,经用标示量或估计效价(AT)校正后,取其对数值(lgPT)参加合并计算。
计算时,令lgPT=M
n次实验结果共n个M值,按(35)式进行X2测验:
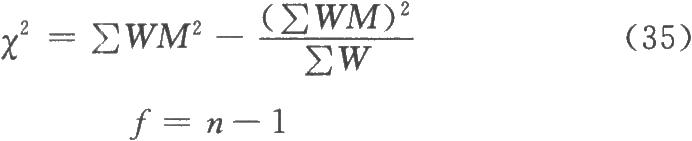
式中W为各次实验结果的权重,相当于各次实验SM平方的倒数,即

按(35)式的自由度(f)查X2值表(表十二),得X2(f)0.05查表值;当X2计算值小于X2(f)0.05查表值时,认为n个实验结果均一,可按(37)式、(38)式、(39)式计算n个M的加权均值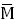 、S
、S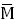 及其FL。
及其FL。
表十二 X2值表(P=0.05)
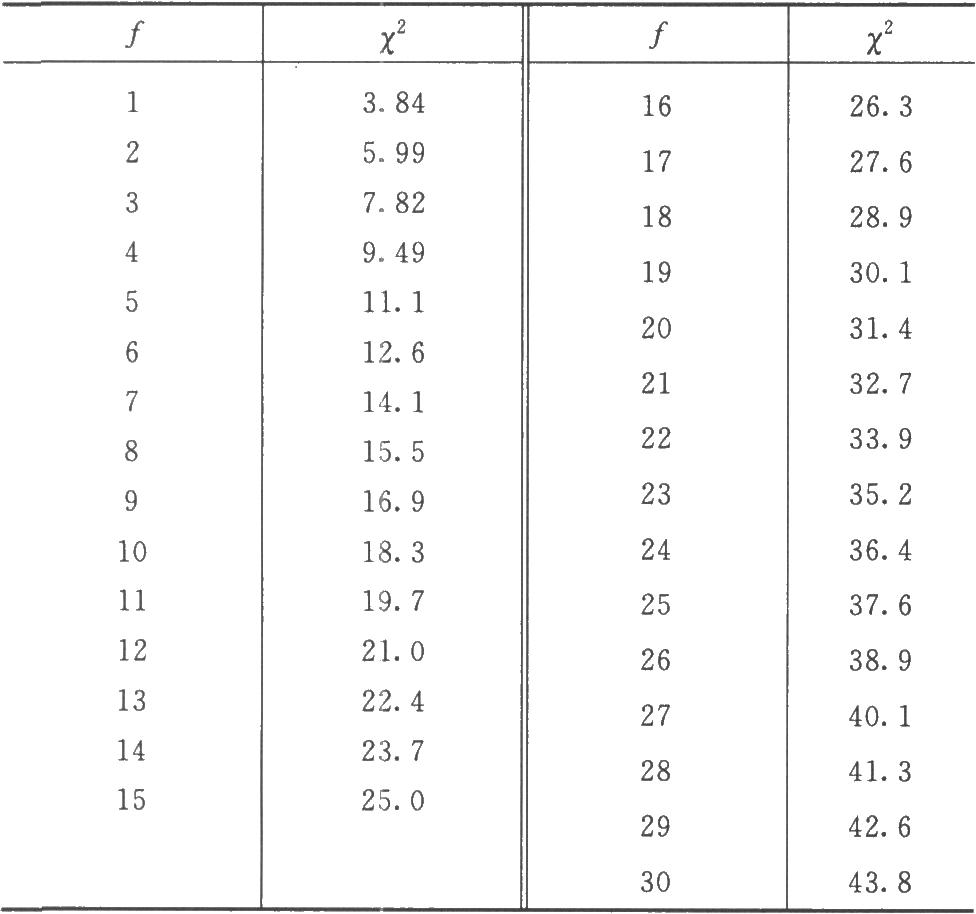
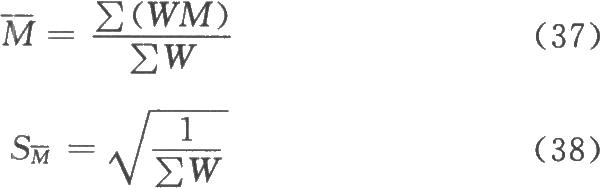
合并计算的自由度(f)是n个实验结果的s2自由度之和。f=∑fi按此f查t值表(表一)得t值。

PT及其可信限按(40)式、(41)式计算:
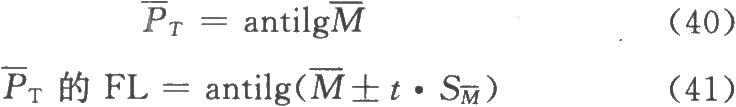
FL%按(8)式计算。
当X2计算值大于X2(f)0.05查表值时,则n个实验结果不均一,可用以下方法进行合并计算。
(1)如为个别实验结果影响n次实验结果的均一性,可以剔除个别结果,将其余均一的结果按以上公式进行合并计算,但剔除个别结果应符合“特异反应剔除”的要求。
(2)如果n次实验结果的不均一性并非个别实验结果的影响,则按(42)式、(43)式计算校正权重W',如经公式(43)计算结果为负值,可以删除减号后面一项,计算近似的S2m和各次实验的W’。用W'和∑W'代替公式(37)、(38)中W和∑W计算M、SM,再按(39)式、(40)式、(41)式计算M的FL、PT及其FL。
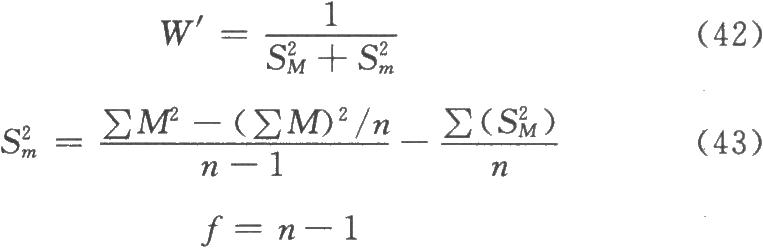
例6 肝素钠5次测定结果的合并计算测定结果见表6-1。
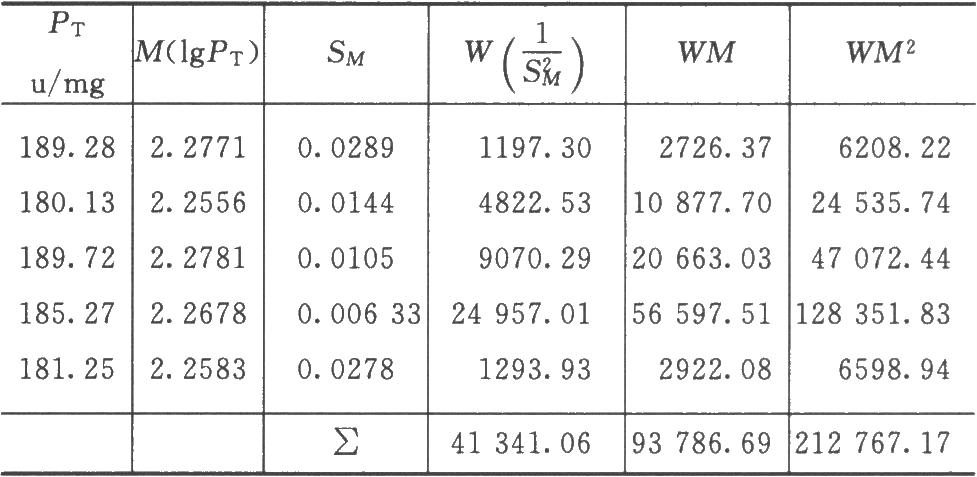
按(35)式计算:
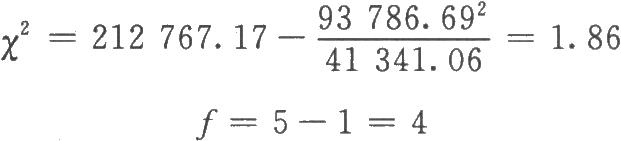
查表十二,X2(4)0.05=9.49
X2计算值1.86
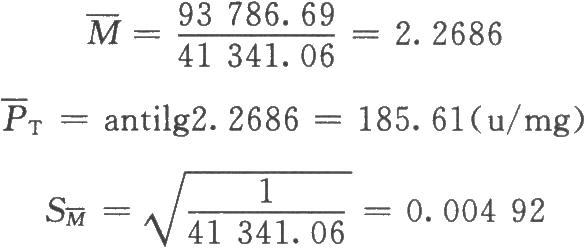
5次实验均用(3.3)法,随机设计,每剂5管,各次实验s2的自由度fi均为:fi=29-5=24。
合并计算的自由度f=5×24=120,t=1.96

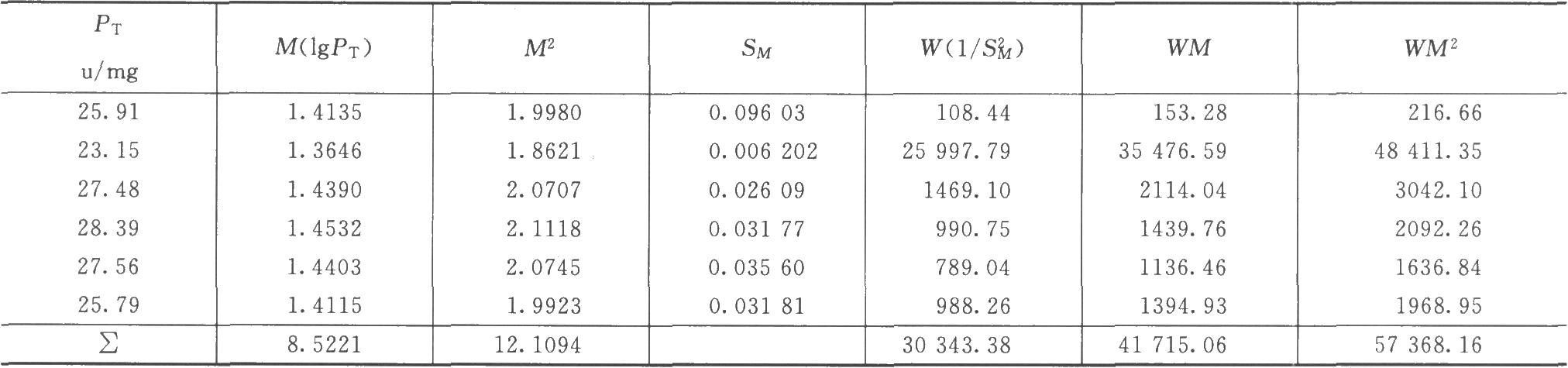
按(35)式:

X2计算值19.70> X2(5)0.05查表值,6次结果不均一,经特异反应剔除计算(公式10),无个别删除结果。
按(42)式、(43)式计算:

计算结果为负数,可删除减号后面项,S2m=0.001007。
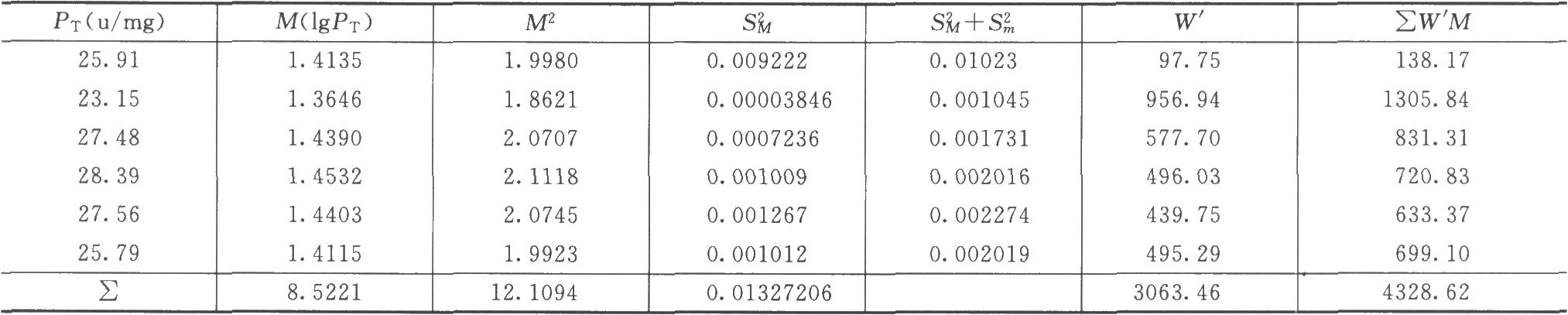
计算各次实验结果的差方S2M、差方和(S2M+S2m)、校正权重W'、∑W'M,见表7-2。
表7-2 胰岛素测定结果不均一时计算表
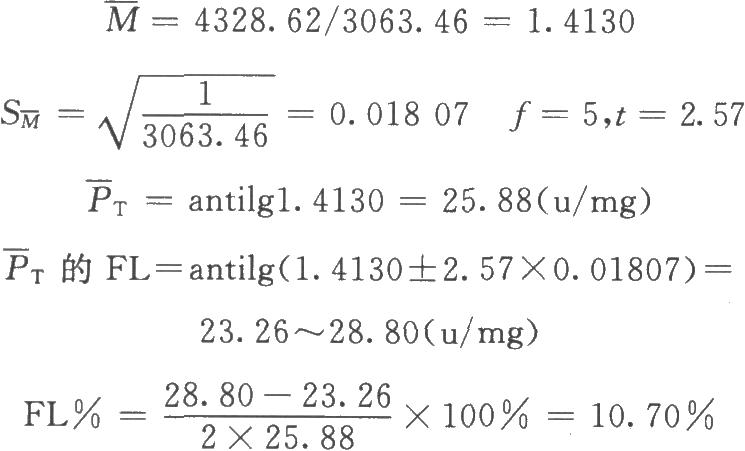
5 五、符号
A SM计算公式中的数值
C 缺项所在列各反应值之和
dS1,dS2…标准品的各剂量dT1,dT2…供试品的各剂量F两方差值之比,用于方差分析等
FL 可信限
FL% 可信限率
f 自由度
G 缺项补足式中除缺项外各反应值之和
g 回归的显著性系数
I 相邻高低剂量比值的对数,I=lgr
J1,J2…特异反应剔除用的J值
K S和T的剂量组数和
k·k' S或T的剂量组数
M S和T的对数等反应剂量之差,即效价比值(R)的对数,M=lgR。合并计算中M=lgPT
n S和T反应个数之和
nS 最小效量法S反应的个数
nT 最小效量法T反应的个数
P 概率
PT、PU 供试品(T、U)的测得效价
R 缺项所在行反应值之和
S1,S2… 平行线测定标准品(S)各剂量组反应值之和,等于S各剂量组的∑y(k)
SM M的标准误
S2 实验的误差项
S2m 合并计算中各次实验间的差方
T 供试品
T1,T2… 平行线测定供试品(T)各剂量组反应值之和,相当于T各剂量组的∑y(k)
t 可信限计算用t值,见表一
U 供试品的另一符号
U1,U2… 平行线测定供试品(U)各剂量组反应值之和,相当于U各剂量组的∑y(k)
u 供试品的效价单位
W 合并计算中为各次实验结果的权重
W' 合并计算中各次实验结果的校正权重
WC 权重系数
nWC 权重
x 对数剂量,x=lgd
XS S的对数剂量或S的对数最小效量
XT T的对数剂量或T的对数最小效量
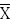 S 直线测定法中,S组对数最小效量的均值
S 直线测定法中,S组对数最小效量的均值
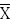 T 直接测定法中,T组对数最小效量的均值
T 直接测定法中,T组对数最小效量的均值
ya、ym 特异反应所在组的两极端值
∑ 总和
X2 卡方
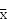 T
T