奈韦拉平药典标准
品名
中文名
奈韦拉平
汉语拼音
Naiweilaping
英文名
Nevirapine
结构式
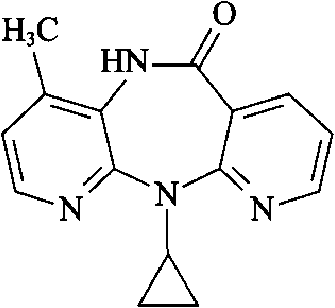
分子式与分子量
C15H14N4O 266.30
来源(名称)、含量(效价)
本品为11-环丙基-5,11-二氢-4-甲基-6H-二吡啶并[3,2,-b:2',3'-e] [1,4]二氮杂䓬-6-酮。按干燥品计算,含C15H14N4O应为98.0%~102.0%。
性状
本品为白色或类白色结晶性粉末;无臭。
本品在三氯甲烷中溶解,在乙醇或甲醇中微溶,在水中几乎不溶。
鉴别
(1)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(2)本品的红外光吸收图谱应与对照的图谱(《药品红外光谱集》1159图)一致。
检查
有关物质
取含量测定项下的供试品贮备溶液,作为供试品溶液;精密量取适量,用流动相稀释制成每1ml中约含奈韦拉平2.5μg的溶液,作为对照溶液。照含量测定项下的色谱条件,取对照溶液20μl注入液相色谱仪,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的20%,再精密量取上述两种溶液各20μl,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的3倍。供试品溶液的色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积的0.4倍(0.2%),各杂质峰面积的和不得大于对照溶液主峰面积(0.5%)。
干燥失重
取本品,在105℃干燥至恒重,减失重量不得过0.5%(2010年版药典二部附录Ⅷ L)。
炽灼残渣
取本品1.0g,依法检查(2010年版药典二部附录Ⅷ N),遗留残渣不得过0.1%。
重金属
取炽灼残渣项下遗留的残渣,依法检查(2010年版药典二部附录ⅧH 第二法),含重金属不得过百万分之十。
含量测定
照高效液相色谱法(2010年版药典二部附录Ⅴ D)测定。
色谱条件与系统适用性试验
用十八烷基硅烷键合硅胶为填充剂;以甲醇-水(33:67)为流动相;检测波长为220nm。理论板数按奈韦拉平峰计算不低于2000。
测定法
取本品约50mg,精密称定,置100ml量瓶中,加甲醇30ml使溶解,用水稀释至刻度,摇匀,作为供试品贮备溶液;精密量取适量,加流动相定量稀释制成每1ml中约含50μg的溶液,精密量取20μl注入液相色谱仪,记录色谱图;另取奈韦拉平对照品,同法测定。按外标法以峰面积计算,即得。
类别
抗病毒药。
贮藏
遮光,密封保存。
制剂
奈韦拉平片
版本
《中华人民共和国药典》2010年版 第二增补本