肿瘤(tumor,neoplasm)是一种常见病、多发病,其中恶性肿瘤是目前危害人类健康最严重的一类疾病。在欧美一些国家,恶性肿瘤的死亡率仅次于心血管系统疾病而居第二位。根据我国1992年卫生事业发展情况统计公报,城市地区居民恶性肿瘤死亡率居死因第一位,为123.92/10万,基中男性为151.08/10万,女性为95.12/10万。农村地区居民恶性肿瘤死亡率居第死因第二位,为101.39/10万。其中男性为125.79/10万,女性为78.85/10万。随着我国人口老龄化的进程,加之城市人口比例逐年增高,城镇工业生产迅速发展,环境污染日益严重,吸烟等不良生活习惯相当普遍,如果不采取积极的宣传教育措施,恶性肿瘤的危害性还将日益增加。我国最为常见和危害性严重的肿瘤为肺癌、鼻咽癌、食管癌、胃癌、大肠癌、肝癌、乳腺癌、宫颈癌、白血病及淋巴瘤等。特别是肺癌发生率近年来有明显的增加,值得重视。这些肿瘤的病因学、发病学及其防治,均应为我国肿瘤研究的重点。
肿瘤的概念
肿瘤是机体在各种致瘤因素作用下,局部组织的细胞在基因水平上失掉了对其生长的正常调控,导致异常增生而形成的新生物。这种新生物常形成局部肿块,因而得名。
正常细胞转变为肿瘤细胞后就具有异常的形态、代谢和功能,并在不同程度上失去了分化成熟的能力。它生长旺盛,并具有相对的自主性,即使后来致瘤因素已不存在时,仍能持续性生长,不仅与机体不协调,而且有害无益。
机体在生理状态下以及在炎症、损伤修复时的病理状态下也常有组织、细胞的增生。但一般来说,这类增生有的属于正常新陈代谢所需的细胞更新;有的是针对一定刺激或损伤的适应性反应,皆为机体生存所需。再者,所增生的组织能分化成熟,并能恢复原来正常组织的结构和功能。而且这类增生是有一定限度的,一旦增生的原因消除后就不再继续增生。但肿瘤性增生却与此不同,二者有着本质上的区别。
根据肿瘤生物学特性及其对机体危害性的不同,一般分为良性和恶性肿瘤两大类。这种分类在肿瘤的诊断、治疗和判断预后上均有十分重要的意义。
肿瘤的一般形态和结构
肿瘤的肉眼观形态
在肉眼观上,肿瘤的形态多种多样,并可在一程度上反映肿瘤的良恶性。
肿瘤的数目和大小肿瘤的大小不一,通常一个,有时可为多个。小者极小甚至在显微镜下才能发现,如原位癌(carcinoma in situ);大者很大,可重达数公斤乃至数十公斤。一般说,肿瘤的大小与肿瘤的性质(良、恶性)、生长时间和发生部位有一定的关系。生长于体表或大的体腔(如腹腔)内的肿瘤有时可长得很大;生长于狭小腔道(如颅腔,椎管)内的肿瘤则一般较小。大的肿瘤通常生长缓慢,生长时间较长,且多为良性。恶性肿瘤生长迅速,短期内即可带来不良后果,故一般不致长得很大。
肿瘤的形状 肿瘤的形状多种多样,有乳头状、菜花状、绒毛状、蕈状、息肉状、结节状、分叶状、浸润性包块状、弥漫性肥厚状、溃疡状和囊状等(图1)。肿瘤形状上的差异一般与其发生部位、组织来源、生长方式和肿瘤的良恶性质密切相关。
肿瘤的颜色 一般肿瘤的切面多呈灰白或灰红色,但可因其含血量的多寡、有无变性、坏死、出血,以及是否含有色素等而呈现各种不同的色调。有时可从肿瘤的色泽大致推测其为何种肿瘤,如血管瘤多呈红色或暗红色,脂肪瘤呈黄色,黑素瘤多呈黑色,绿色瘤呈绿色等。
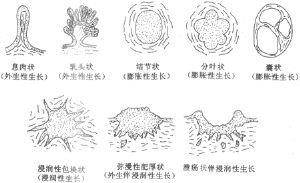
图1 肿瘤的外形和生长方式模式图
肿瘤的硬度肿瘤一般较其来源组织的硬度增大,其硬度与肿瘤的种类、瘤实质与间质的比例以及有无变性坏死等有关。如骨瘤很硬,脂肪瘤质软;实质多于间质的肿瘤一般较软,反之则较硬;瘤组织发生坏死时变软,有钙质沉着(钙化)或骨质形成(骨化)时则变硬。
肿瘤的组织结构
肿瘤的组织多种多样,但概而言之,任何一个肿瘤的组织成分都可概括为实质和间质两部分。
肿瘤的实质 肿瘤实质是肿瘤细胞的总称,是肿瘤的主要成分。肿瘤的生物学特点以及每种肿瘤的特殊性都是由肿瘤的实质决定的。机体内几乎任何组织都可发生肿瘤,因此肿瘤实质的形态也多种多样,通常根据肿瘤的实质形态来识别各种肿瘤的组织来源(histogenesis),进行肿瘤的分类、命名和组织学诊断;并根据其分化成熟程度和异型大小来确定肿瘤的良恶性。
肿瘤的间质 肿瘤的间质成分不具特异性,起着支持和营养肿瘤实质的作用,一般系由结缔组织和血管组成,有时还可有淋巴管。通常生长快的肿瘤,其间质血管多较丰富而结缔组织较少;生长缓慢的肿瘤,其间质血管则较少。此外,肿瘤间质内往往有或多或少的淋巴细胞等单个核细胞浸润,这是机体对肿瘤组织的免疫反应。近年来在肿瘤结缔组织间质中除见纤维母细胞外,尚出现肌纤维母细胞(myofibroblast)。此种细胞兼具纤维母细胞和平滑肌细胞的一些形态和功能特点,细胞呈梭形。电镜下,胞浆内除见丰富的粗面内质网外,在细胞膜下可见平滑肌微丝。此种细胞既能产生胶原纤维,又有收缩功能。由于此种细胞增生、收缩和形成胶原纤维包绕肿瘤细胞,可能对肿瘤细胞的浸润过程有所阻抑,并限制瘤细胞的活动和遏止瘤细胞侵入血管内或淋巴管内,从而减少播散机会。此外,此种细胞的增生还可解释临床上所见乳腺癌时的乳头回缩,食管癌及肠癌所致的管壁僵硬和狭窄。
肿瘤的异型性
肿瘤组织无论在细胞形态和组织结构上,都与其发源的正常组织有不同程度的差异,这种差异称为异型性(atypia)。肿瘤组织异型性的大小反映了肿瘤组织的成熟程度(即分化程度,在此指肿瘤的实质细胞与其来源的正常细胞和组织在形态和功能上的相似程度)。异型性小者,说明它和正常组织相似,肿瘤组织成熟程度高(分化程度高);异型性大者,表示瘤组织成熟程度低(分化程度低)。区别这种异型性的大小是诊断肿瘤,确定其良、恶性的主要组织学依据。恶性肿瘤常具有明显的异型性。
由未分化细胞构成的恶性肿瘤也称为间变性肿瘤。间变(anaplasia)一词的原意是指“退性发育”,即去分化,指已分化成熟的细胞和组织倒退分化,返回原始幼稚状态。现已知,绝大部分的未分化的恶性肿瘤起源于组织中的干细胞丧失了分化能力,而并非是已经分化的特异细胞去分化所致。在现代病理学中,间变指的是恶性肿瘤细胞的缺乏分化。间变性的肿瘤细胞具有明显的多形性(pleomorphism,即瘤细胞彼此在大小和形状上的变异)。因此,往往不能确定其组织来源。间变性肿瘤几乎都是高度恶性的肿瘤,但大多数恶性肿瘤都显示某种程度的分化。
肿瘤组织结构的异型性
良性肿瘤瘤细胞的异型性不明显,一般都与其发源组织相似。因此,这种肿瘤的诊断有赖于其组织结构的异型性。例如纤维瘤的细胞和正常纤维细胞很相似,只是其排列与正常纤维组织不同,呈编织状。恶性肿瘤的组织结构异型性明显,瘤细胞排列更为紊乱,失去正常的排列结构层次。例如,从纤维组织发生的恶性肿瘤—纤维肉瘤,瘤细胞很多,胶原纤维很少,排列很紊乱,与正常纤维组织的结构相差较远;从腺上皮发生的恶性肿瘤—腺癌,其腺体的大小和形状十分不规则,排列也较乱,腺上皮细胞排列紧密重叠或呈多层,并可有乳头状增生。
肿瘤细胞的异型性
良性肿瘤细胞的异型性小,一般与其发源的正常细胞相似。恶性肿瘤细胞常具有高度的特异性,表现为以下特点:
1.瘤细胞的多形性 即瘤细胞形态及大小不一致。恶性肿瘤细胞一般比正常细胞大,各个瘤细胞的大小和形态又很不一致,有时出现瘤巨细胞(图2)。但少数分化很差的肿瘤,其瘤细胞较正常细胞小、圆形,大小也比较一致。
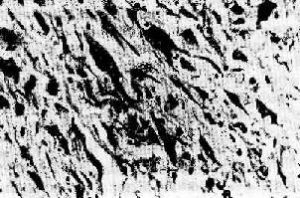
图2 横纹肌肉瘤
瘤细胞大小、形状不一,并有瘤巨细胞出现
即瘤细胞核的大小、形状及染色不一致。细胞核的体积增大(核肥大),胞核与细胞浆的比例比正常增大(正常为1:4~6,恶性肿瘤细胞则接近1:1),核大小及形状不一,并可出现巨核、双核、多核或奇异形的核,核染色深(由于核内DAN增多),染色质呈粗颗粒状,分布不均匀,常堆积在核膜下,使核膜显得增厚。核仁肥大,数目也常增多(可达3~5个)。核分裂像常增多,特别是出现不对称性、多极性及顿挫性等病理性核分裂像时,对于诊断恶性肿瘤具有重要的意义。恶性肿瘤细胞的核异常改变多与染色体呈多倍体(polyploidy)或非整倍体(aneuploidy)有关。
胞浆的改变
由于胞浆内核蛋白体增多,胞浆呈嗜碱性。并可因为瘤细胞产生的异常分泌物或代谢产物而具有不同特点,如激素、粘液、糖原、脂质、角质和色素等。
上述瘤细胞的形态,特别是胞核的多形性常为恶性肿瘤的重要特征,在区别良恶性肿瘤上有重要意义。
肿瘤细胞超微结构的异型性
由于肿瘤类型不同,瘤细胞的超微结构亦有差异。一般说来,良性肿瘤细胞的超微结构基本上与其起源细胞相似。恶性肿瘤细胞根据分化的高低而表现出不同程度的异型性。总的说来,恶性肿瘤细胞的核通常绝对或相对明显增大,核膜可有内陷或外凸,从而使核形不规则甚至形成怪形核。核仁体积增大,数目增多,形状亦可不规则,位置往往靠边。染色质可表现为异染色质增加,凝集成块状散在或(和)边集在核膜下。此即光镜下所见的深染核和核膜增厚;也可表现为常染色质为主,即光镜下所见染色质呈细颗粒状的淡染核。胞浆内的细胞器常有数目减少、发育不良或形态异常,这在分化低的恶性肿瘤细胞更为明显。胞浆内主要见游离的核蛋白体,而其他细胞器大为减少。说明瘤细胞主要合成供自身生长的蛋白质,而丧失其分化的功能,这与瘤细胞生长迅速和恶性程度高有关。溶酶体在侵袭性强的瘤细胞中常有增多,它可释放出大量水解酶,为瘤细胞的浸润开路。细胞间连接常有减少,这在分化低的癌更为突出。可引起细胞间粘着松散,有利于细胞浸润生长。有些在一般情况下在细胞膜表面无微绒毛的瘤细胞也可出现一些不规则微绒毛,这有利于营养物质的吸收,但有碍于细胞间的紧密接触,从而减弱接触抑制,有利于细胞增殖和浸润。瘤细胞的排列结构在分化低的肿瘤也可丧失其原具有的特征改变,例如腺癌细胞可失掉形成腺体的特征而呈弥散排列。因此,恶性肿瘤的超微结构异型性的改变,除了瘤细胞本身的改变外,还可有排列结构的改变。
肿瘤细胞的代谢特点
肿瘤组织比正常组织代谢旺盛,尤以恶性肿瘤理更为明显。其代谢特点与正常组织相比并无质的差别,但在一定程度上反映了瘤细胞分化不成熟和生长旺盛。
核酸代谢
肿瘤组织合成DNA和RNA的聚合酶活性均较正常组织高,与此相应,核酸分解过程明显降低,故DNA和RNA的含量在恶性肿瘤细胞均明显增高。DNA与细胞的分裂和繁殖有关,RNA与细胞的蛋白质合成及生长有关。因此,核酸增多是肿瘤迅速生长的物质基础。
蛋白质代谢
肿瘤组织的蛋白质合成及分解代谢都增强,但合成代谢超过分解代谢,甚至可夺取正常组织的蛋白质分解产物,合成肿瘤本身所需要的蛋白质,结果可使机体处于严重消耗的恶病质(cachexia)状态。肿瘤的分解代谢表现为蛋白质分解为氨基酸的过程增强,而氨基酸的分解代谢则减弱,可使氨基酸重新用于蛋白质合成。这可能与肿瘤生长旺盛有关。肿瘤组织还可以合成肿瘤蛋白,作为肿瘤特异抗原或肿瘤相关抗原,引起机体的免疫反应。有的肿瘤蛋白与胚胎组织有共同的抗原性,亦称为肿瘤胚胎性抗原。例如肝细胞癌能合成胎儿肝细胞所产生的甲种胎儿蛋白(AFP),此外,卵巢、睾丸含有卵黄囊结构的生殖细胞肿瘤患者血中AFP也有升高;内胚层组织发生的一些恶性肿瘤如结肠瘤、直肠癌等可产生癌胚抗原(CEA);胃癌可产生胎儿硫糖蛋白等。虽然这些抗原并无肿瘤特异性,也不是肿瘤所专有,但检查这些抗原,并结合其他改变可帮助诊断相应的肿瘤和判断治疗后有无复发。
酶系统
肿瘤组织酶活性的改变是复杂的。除了一般在恶性肿瘤组织内氧化酶(如细胞色素氧化酶及琥珀酸脱氢酶)减少和蛋白分解酶增加外,其他酶的改变在各种肿瘤间很少是共同的,而且与正常组织比较只是含量的改变或活性的改变,并非是质的改变。例如前列腺癌的癌组织中酸性磷酸酶明显增加,在前列腺癌伴有广泛骨转移时,患者血清中的酸性磷酸酶也明显增加;骨肉瘤及肝癌时碱性磷酸酶增加,这不但见于肿瘤组织中,还可见于病人的血清中。这些均有助临床诊断。
各种不同组织来源的恶性肿瘤特别是细胞分化原始幼稚者,其酶变化特点主要表现为某些特殊功能的酶接近或完全消失,并因而导致酶谱的一致性。例如分化差的肝癌组织中有关尿素合成的特殊酶系几乎完全消失。其酶谱乃因而趋向与其他癌组织的酶谱一致,与胚胎细胞的酶谱相似。有时还可出现通常所没有的酶。
糖代谢
大多数正常组织在有氧时通过糖的有氧分解获取能量,只有在缺氧时才进行无氧糖酵解。肿瘤组织则即使在氧供应充分的条件下也主要是以无氧糖酵解获取能量。这可能是由于癌细胞线粒体的功能障碍所致,或者与瘤细胞的酶谱变化,特别是与三个糖酵解关键酶(己糖激酶、磷酸果糖激酶和丙酮酸激酶)活性增加和同工酶谱的改变,以及糖异生关键酶活性降低有关。糖酵解的许多中间产物被瘤细胞利用合成蛋白质、核酸及脂类,从而为瘤细胞本身的生长和增生提供了必需的物质基础。
肿瘤的生长与扩散
具有局部浸润和远处转移能力是恶性肿瘤细胞特有的性质。并且是恶性肿瘤威胁病人健康与生命的主要原因。因此对肿瘤生长与扩散的研究已成为肿瘤病理学的重要内容。
肿瘤生长的生物学
典型的恶性肿瘤的自然生长史可以分成几个阶段:细胞的恶性转化→转化细胞的克隆性增生→局部浸润→远处转移。在此过程中,恶性转化细胞的内在特点(如肿瘤细胞倍增时间)和宿主对肿瘤细胞或其产物的反应(如肿瘤血管形成)共同影响肿瘤的生长与演进。
1.肿瘤生长动力学肿瘤的生长速度取决于三个因素:
(1)肿瘤细胞倍增时间:恶性转化细胞的生长周期与正常细胞一样,分为G0、G1、S、G2和M期。多数恶性肿瘤细胞的培增时间并不是想象的那样比正常细胞更快,而是与正常细胞相似或者长于正常细胞。
(2)生长分数(growth fraction);生长分数指肿瘤细胞群体中处于复制阶段(S+G2期)的细胞的比例。在细胞恶性转化的初期,绝大多数的细胞处于复制期,所以生长分数很高。但是随着肿瘤的持续生长,不断有瘤细胞发生分化,离开复制阶段的细胞越来越多,使得大多数肿瘤细胞处于G0期。即使是生长迅速的肿瘤其生长分数也只在20%左右。
(3)瘤细胞的生成与丢失:肿瘤的进行性生长及其生长速度决定于其细胞的生成大于丢失的程度。由于营养供应不足,坏死脱落以及机体抗肿瘤反应等因素的影响,在肿瘤生长过程中,有相当一部分瘤细胞失去生命力。肿瘤细胞的生成与丢失的程度共同影响着肿瘤的生长。在生长分数相对较高的肿瘤,瘤细胞的生成远大于丢失,因此其生长速度比那些细胞生成稍超过丢失的肿瘤要快得多。
肿瘤的细胞动力学概念在肿瘤的化学治疗上有重要的意义。目前几乎所有的化学抗癌药物均针对处于复制期的细胞。因此高生长分数的肿瘤(如高恶性的淋巴瘤)对于化疗特别敏感;常见的实体瘤(如结肠癌)生长分数低,故对治疗出现相对耐药性。临床治疗这些肿瘤的战略是先用放射或手术治疗将肿瘤缩小,使残存的瘤细胞从G0期进入复制期后再用化疗。
2.肿瘤的血管形成 临床与动物实验都证明,如果没有新生的血管供应营养,肿瘤在达到1~2mm的直径或厚度后,即107个细胞左右将不再增大。因此诱导血管的生成能力是恶性肿瘤能生长、浸润与转移的前提之一。现已发现,由肿瘤细胞本身和浸润到肿瘤组织内及其周围的炎细胞(主要是巨噬细胞)能产生一类血管生成因子(angiogenesis factor),如纤维母细胞生长因子(fibroblastic growth factor,FGF)、血小板衍生的内皮细胞生长因子(platelet-derived endothelial cell growth factor,PD-ECGF)、转化生长因子α(transforming growth factor-α,TGF-α)、肿瘤坏死因子α(TNF-α)、血管内皮细胞生长因子(vascular endothelial growth factor,VEGF)等。其中最具有特征性血管生成作用的是由肿瘤细胞产生的FGF,它能通过其受体与相应的靶细胞结合。有增加内皮细胞的化学趋向性、促进血管内皮细胞分裂、毛细血管出芽生长、诱导蛋白溶解酶生成和有利于内皮细胞芽穿透基质等功能。此外,巨噬细胞产生的TNF-α也有促进内皮细胞分裂和刺激其游走的作用。新生的毛细血管既为肿瘤的生长提供了营养,又为肿瘤的转移准备了条件。因此对抑制肿瘤血管生成的研究是当前的研究热点之一。
3.肿瘤的演进与异质化 恶性肿瘤在生长过程中变得越来越富有侵袭性的现象称为肿瘤的演进(progression),包括生长加快、浸润周围组织和远处转移等。这些生物学现象的出现与肿瘤细胞的不同亚克隆在侵袭能力、生长速度、对激素的反应、对抗癌药的敏感性等方面的差异—肿瘤的异质性(heterogeneity)有关。产生这种现象的原因是在肿瘤的生长过程中,可能有附加的基因突变(详见第十五节)作用于不同的瘤细胞,使得瘤细胞的亚克隆获得不同的特性。例如需要较多生长因子的亚克隆可因生长因子缺乏而不能生长,而有些需要较少生长因子的亚克隆在此时即可生长;机体的抗肿瘤反应可杀死那些具有较高的抗原性的亚克隆,而抗原性低的亚克隆则可以躲过机体的免疫监视。由于这些选择,肿瘤在生长过程中能保留那些适应存活、生长、浸润与转移的亚克隆。这就是肿瘤的异质化。
肿瘤的生长方式和扩散
肿瘤的生长速度
各种肿瘤的生长速度有极大的差异,主要决定于肿瘤细胞的分化成熟程度。一般来讲,成熟程度高、分化好的良性肿瘤生长较缓慢,几年甚至几十年。如果其生长速度突然加快,就要考虑发生恶性转变的可能。成熟程度低、分化差的恶性肿瘤生长较快,短期内即可形成明显的肿块,并且由于血管形成及营养供应相对不足,易发生坏死,出血等继发改变。
肿瘤的生长方式
肿瘤可以呈膨胀性、外生性和浸润性生长:
(1)膨胀性生长:这是大多数良性肿瘤所表现的生长方式。由于这种瘤细胞生长缓慢,不侵袭周围正常组织,随着肿瘤体积的逐渐增大,有如逐渐膨胀的气球,向四周组织推挤。因此肿瘤往往呈结节状,周围常有完整的包膜,与周围组织分界清楚(图7-3)。位于皮下者临床触诊时可以推动,容易手术摘除,摘除后也不易复发。虽这种生长方式的肿瘤对局部器官、组织的影响主要为挤压或阻塞,一般均不明显破坏器官的结构和功能。
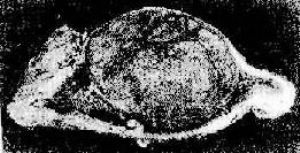
图3 良性肿瘤的膨胀性生长(肾上腺皮质腺瘤)
肿瘤呈卵圆形,有包膜,与周围肾上腺组织分界清楚
(2)外生性生长:发生在体表、体腔表面或管道器官(如消化道,泌尿生殖道等)表面的肿瘤,常向表面生长,形成突起的乳头状、息肉状、蕈状或菜花状的肿物。这种生长方式称为外生性生长。良性肿瘤和恶性肿瘤都可呈外生性生长。但恶性肿瘤在外生性生长的同时,其基底部往往也呈浸润性生长,又由于其生长迅速,血液供应不足,这种外生性肿物容易发生坏死脱落而形成底部高低不平、边缘隆起的癌性溃疡。
(3)浸润性生长:为大多数恶性肿瘤的生长方式。瘤细胞分裂增生,侵入周围组织间隙、淋巴管或血管内,如树根之长入泥土,浸润并破坏周围组织。因而此类肿瘤没有包膜,与邻近的正常组织紧密连接在一起而无明显界限(图4)。临床触诊时,肿瘤固定不活动。手术切除这种肿瘤时,切除范围比肉眼所见肿瘤范围为大,因为这些部位也可能有肿瘤细胞的浸润。

图4 恶性肿瘤的浸润性生长(食管鳞状细胞癌)
癌细胞形成大小、形状不一的细胞巢,浸润于管壁组织(包括肌层)间隙内
肿瘤的扩散
具有浸润性生长的恶性肿瘤,不仅可以在原发部位继续生长、蔓延(直接蔓延)而且还可以通过多种途径扩散至身体其他部位(转移)。
(1)直接蔓延:随着肿瘤的不断长大,瘤细胞常常连续不断地沿着组织间隙、淋巴管、血管或神经束衣侵入并破坏邻近正常器官或组织,并继续生长,称为直接蔓延。例如晚期子宫颈癌可蔓延至直肠和膀胱;晚期乳腺癌可穿过胸肌和胸腔甚至达肺。
(2)转移(metastasis):瘤细胞从原发部位侵入淋巴管、血管或体腔,被带到他处而继续生长,形成与原发瘤同样类型的肿瘤,这个过程称为转移。所形成的肿瘤称为转移瘤或继发瘤。良性肿瘤不转移,只有恶性肿瘤才可能发生转移。常见的转移途径有以下几种:
1)淋巴道转移:瘤细胞侵入淋巴管(图5)后,随淋巴流首先到达局部淋巴结。例如乳腺外上象限发生的乳腺癌首先到达同侧腋窝淋巴结;肺癌首先到达肺门淋巴结。瘤细胞到达局部淋巴结后,先聚集于边缘窦,以后生长繁殖而累及整个淋巴结(图6),使淋巴结肿大,质地变硬,切面常呈灰白色。有时有转移的淋巴结由于瘤组织侵出被膜而互相融合成团块。局部淋巴结发生转移后,可继续转移至下一站的其他淋巴结,最后可经胸导管进入血流再继发血道转移。
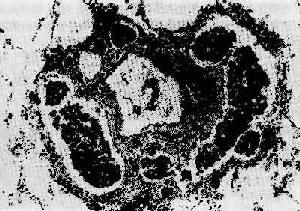
图5 肿瘤的淋巴道转移
肺内血管周围淋巴管扩张,充满瘤细胞团(瘤细胞栓子)
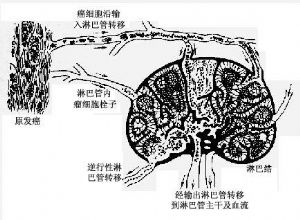
图6癌的淋巴道转移模式图
—→淋巴流向 ……→癌细胞流向
2)血道转移:瘤细胞侵入血管后可随血流到达远隔器官继续生长,形成转移瘤。由于动脉壁较厚,同时管内压力较高,故瘤细胞多经小静脉入血。少数亦可经过淋巴管入血。血道转移的运行途径与血栓栓塞过程相同,即侵入体循环静脉的肿瘤细胞经右心到肺,在肺内形成转移瘤,例如骨肉瘤等的肺转移;侵入门静脉系统的肿瘤细胞,首先形成肝内转移,例如胃、肠癌的肝转移等;侵入肺静脉的肿瘤细胞或肺内转移瘤通过肺毛细血管而进入肺静脉的瘤细胞,可经左心随主动脉血流到达全身各器官,常见转移脑、骨、肾及肾上腺等处。因此,这些器官的转移瘤常发生在肺已有转移之后。此外,侵入胸、腰、骨盆静脉的肿瘤细胞,也可以通过吻合支进入脊椎静脉丛(Batson脊椎静脉系统),例如前列腺癌就可通过此途径转移到脊椎,进而转移到脑,这时可不伴有肺的转移。
血道转移虽然可见于许多器官,但最常见的是肺,其次是肝。故临床上判断有无血道转移,以确定患者的临床分期和治疗方案时,作肺部的X线检查及肝的超声等影像学探查是非常必要的。转移瘤在形态上的特点是边界清楚并常为多个散在分布的结节,且多接近器官的表面(图7-7)。位于器官表面的转移瘤,由于瘤结节中央出血、坏死而下陷,可形成“癌脐”。
3)种植性转移:体腔内器官的肿瘤蔓延而于器官表面时,瘤细胞可以脱落并象播种一样,种植在体腔和体腔内各器官的表面,形成多数的转移瘤。这种转移的方式称为种植性转移或播种。种植性转移常见于腹腔器官的癌瘤。如胃癌破坏胃壁侵及浆膜后,可种植到大网膜、腹膜、腹腔内器官表面甚至卵巢等处。肺癌也常在胸腔内形成广泛的种植性转移。浆膜腔的种植性转移每伴有浆液性血性积液。这是由于浆膜下淋巴管或毛细血管被癌栓阻塞,或浆膜受癌的刺激,使其内毛细血管的通透性增加而致渗出增多,并由于血管被癌细胞破坏而引起出血这故。抽吸积液作细胞学检查常可查见癌细胞。脑部的恶性肿瘤,如小脑的髓母细胞瘤(medulloblastoma)亦可经脑脊液转移到脑的其他部位或脊髓,形成种植性转移。值得注意的是,手术也可能造成种植转移,应注意尽量避免。
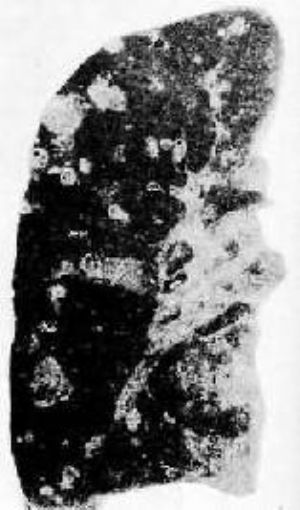
图7 肺内的血道转移性癌
肺的切面上可见多数大小不等的图形癌结节,边界清楚
恶性肿瘤的浸润和转移机制
(1)局部浸润:恶性肿瘤局部浸润的机制目前尚未十分明了,但已知是一个由一系列步骤组成的复杂过程。前面提到的浸润能力强的瘤细胞亚克隆的出现和肿瘤血管形成对此都起着重要的作用。局部浸润发生时,由细胞粘附分子(cell adhesion molecules)介导的肿瘤细胞彼此之间的粘附力减弱和瘤细胞与基质的附着力增加是近年来关于侵润机制研究的重点。已有资料显示,在动物高浸润性的肿瘤细胞株,其瘤细胞表面的一种粘附分子——上皮粘连素(E—cadherin)的表达减少,而如将编码上皮粘连素DNA插入到瘤细胞基因组中,则可使其丧失转移和浸润能力。瘤细胞彼此分散才能侵入细胞外基质(extracellular matrix,ECM)。细胞外基质在机体内分隔上皮组织和结缔组织,包括基底膜和间质性结缔组织,主要是由胶原、糖蛋白和蛋白多糖组成。正常上皮细胞与基质的结合是通过存在于上皮细胞膜表面的整合素(integrin)的粘附分子与存在于基质中的其配体的结合来实现的。
癌细胞的ECM主要成成分——基底膜的侵袭是一主动过程,可分为三个步骤:①癌细胞附着于基底膜(attachment):正常上皮细胞具有的一种整合素——层粘连蛋白(laminin,LN)的受体,只分布在细胞的基底面,能与基底膜的LN分子结合而使上皮细胞附着。而癌细胞则有更多的LN受体,分布于癌细胞的整个表面,使癌细胞更容易与基底膜粘附。例如已发现,人的侵润性乳腺癌细胞与LN的结合能力为正常或良性乳腺上皮细胞的50倍,这类病人发生淋巴结转移的机会大大高于LN受体较少的乳腺癌病人。纤维粘连蛋白(fibronectin,FN)也是基底膜的成分,可与上皮细胞表面的一种整合素——FN受体结合而使细胞附着于基底膜。癌细胞FN受体表达增加和其侵袭性之间也存在于与LN类似的关系;②细胞外基质的降解(degradation);在癌细胞与基底膜紧密接触4~8小时后,ECM的成分,如LN、FN、蛋白多糖和胶原纤维(Ⅳ型)可被癌细胞直接分泌的蛋白溶解酶(包括Ⅳ型胶原酶、尿激酶型胞浆素原活化物、组织蛋白酶D等)溶解,使基底膜产生局部的缺损。癌细胞也可诱导宿主细胞(如纤维母细胞)产生蛋白酶,使ECM溶解。Ⅳ型胶原酶是一种金属蛋白酶,能分解上皮和血管基底膜的Ⅳ型胶原纤维,已有报告指出在乳腺癌和胃癌细胞有这种酶的过度表达。动物实验还发现Ⅳ型胶原酶的抑制剂可以大大减少转移的发生;③癌细胞的移出(migration);癌细胞通过被溶解的基底膜缺损处游出是借助于自身的阿米巴运动。近来发现肿瘤细胞的衍生的细胞激肽,如自分泌移动因子(autocrine motility factor)可介导瘤细胞的移动。基质成分(如胶原、LN)的降解产物和某些生长因子(如胰岛素样生长因子Ⅰ和Ⅱ)对癌细胞有化学趋向性。癌细胞穿过基底膜后,重复上述步骤进一步溶解间质性的结缔组织,在间质中移动。到达血管壁时,可以以同样方式穿过血管的基底膜进入血管(图7-8)。
(2)血行播散:进入血管的癌细胞形成新的转移灶的可能性小于千分之一,因单个癌细胞进入血管后绝大多数为机体的免疫细胞消灭。但被血小板凝集成团的癌细胞形成的瘤栓则不易被消灭,并可与形成栓塞处的血管内皮细胞粘附,然后以前述机制穿过血管内皮和基底膜,形成新的转移灶(图7-8)。由于肿瘤的异质化而选择出的高侵袭性的瘤细胞亚克隆,尤其容易形成广泛的血行播散。
转移的发生不是随机的。早在1889年Paget在对700多侧乳腺癌的转移进行分析后,就发现有明显的器官倾向性,并提出有名的“种子和土壤”学说。血行转移的位置和器官分布,在某些肿瘤具有特殊的亲和性,如肺癌易转移到肾上腺和脑;甲状腺癌、肾癌和前列腺癌易转移到骨;乳腺癌常转移到肺、肝、骨、卵巢和肾上腺等。产生这种现象的原因还不清楚,可能是由于这些器官的血管内皮上有能与进入血循环的癌细胞表面的粘附分子特异性结合的配体(如血管细胞粘附分子),或者由于靶器官能够释放某些吸引癌细胞的化学吸引物质(如胰岛素样生长因子Ⅰ和Ⅱ)。此外,转移瘤在某些组织或器官中不易形成,也可能与这些器官或组织的环境不适合肿瘤的生长有关。如脾虽然血液循环丰富但转移癌少见,可能是因为脾是免疫器官;横纹肌转移瘤很少,可能是因为肌肉经常收缩使瘤细胞不易停留或肌肉内乳酸含量过高,不利于肿瘤生长。
(3)肿瘤转移的分子遗传学:目前尚发现一个单独的转移基因,但已发现一种肿瘤抑制基因——nm23的表达水平与肿瘤的侵袭和转移能力之间存在有意义的关系。在小鼠模型中,nm23的表达高者具有低转移性;nm23表达低10倍者伴有高转移。人类的nm23基因定位于第17位号染色体。在侵袭性强的肿瘤中nm23基因丢失。临床上对人乳腺癌的观察发现,淋巴结转移少于三个者,nm23蛋白表达水平高;而有广泛转移者nm23蛋白表达的水平一般均低。如能将nm23蛋白作为标记物来预测转移并且在治疗上用于抑制转移,将是肿瘤治疗的一个突破。现此问题正在积极研究中。
肿瘤的分级与分期
肿瘤的分级(grading)和分期(staging)一般都用于恶性肿瘤。恶性肿瘤是根据其分化程度的高低、异型性的大小及核分裂像的多少来确定恶性程度的级别。近年来较多的人倾向于用简明的、较易掌握的三级分级法,即Ⅰ级为分化良好的,属低度恶性;Ⅱ级为分化中等的,属中度恶性;Ⅲ级为分化低的,属高度恶性。这种分级法虽有其优点,对临床治疗和判断预后也有一定意义。但缺乏定量标准,也不能排除主观因素的影响。因此,如何建立精确的分级标准还待进一步研究。
肿瘤的分期目前有不同的方案,其主要原则是根据原发肿瘤的大小、浸润的深度、范围以及是否累及邻近器官、有无局部和远处淋巴结的转移、有无血源性或其他远处转移等来确定肿瘤发展的程期或早晚。
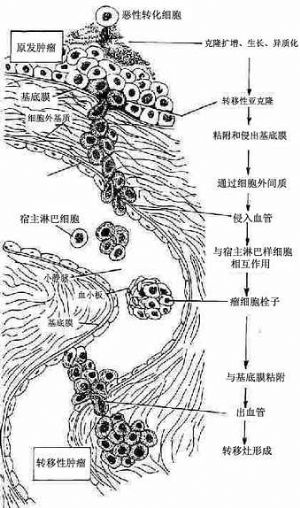
图8 恶性肿瘤浸润和转移机制
恶性肿瘤细胞侵出基底膜进入细胞外间质,侵入血管并形成新的转移灶(采自Basic Pathology)
肿瘤的分级和分期对临床上制定治疗方案和估计预后有参考价值,特别是肿瘤的分期更为重要,但是必须结合各种恶性肿瘤的生物学特性以及病人的全身情况等综合考虑。
肿瘤对机体的影响
肿瘤因其良恶性的不同,对机体的影响也有所不同。
良性肿瘤
因其分化较成熟,生长缓慢,停留于局部,不浸润,不转移,故一般对机体的影响相对较小,主要表现为局部压迫和阻塞症状。其影响的发生主要与其发生部位和继发变化有关。如体表良性瘤除少数可发生的局部症状外,一般对机体无重要影响;但若发生在腔道或重要器官,也可引起较为严重的后果,如消化道良性肿瘤(如突入肠腔的平滑肌瘤),有时引起肠梗阻或肠套叠;颅内的良性瘤(如脑膜瘤、星形胶质细胞瘤)可压迫脑组织阻塞脑室系统而引起颅内压升高和相应的神经系统症状。良性肿瘤有时可发生继发性改变,亦可对机体带来程度不同的影响,如肠的腺瘤性息肉、膀胱的乳头状瘤等表面可发生溃疡而引起出血和感染。此外,内分泌腺的良性肿瘤则常因能引起某种激素分泌过多而产生全身性影响,如垂体前叶的嗜酸性腺瘤(acidophil adenoma)可引起巨人症(gigantism)或肢端肥大症(acromegaly);胰岛细胞瘤分泌过多的胰岛素,可引起阵发性血糖过低等。
恶性肿瘤
恶性肿瘤由于分泌不成熟、生长较快,浸润破坏器官的结构和功能,并可发生转移,因而对机体的影响严重。恶性瘤除可引起与上述良性瘤相似的局部压迫和阻塞症状外,发生于消化道者更易并发溃疡、出血、甚致穿孔,导致腹膜炎,后果更为严重。有时肿瘤产物或合并感染可引起发热。肿瘤浸润、压迫局部神经还可引起顽固性疼痛等症状。恶性肿瘤的晚期患者,往往发生恶病质(cachexia),可致患者死亡。恶病质是指机体严重消瘦、无力、贫血和全身衰竭的状态,其发生机制尚未完全阐明,可能由于缺乏食欲,进食减少、出血、感染、发热或因肿瘤组织坏死所产生的毒性产物等引起机体的代谢紊乱所致。此外,恶性肿瘤的迅速生长,消耗机体大量的营养物质,以及由于晚期癌瘤引起的疼痛,影响患者的进食及睡眠等,也是招致恶病质的重要因素。近年来发现巨噬细胞产生的肿瘤坏死因子(TNF)可降低食欲和增加分解代谢,与恶病质的发生有一定关系。
近年来相继发现一些非内分泌腺肿瘤能产生和分泌激素或激素类物质,如促肾上腺皮质激素(ACTH)、甲状旁腺素(PTH)、胰岛素、抗利尿激素(ADH)、人绒毛膜促性腺激素(HCG)、促甲状腺激素(TSH)、生长激素(GH)、降钙素(calcitonin)等十余种,可引起内分泌紊乱的临床症状。此类肿瘤称为异位内分泌肿瘤,其所引起的临床症状称为异位内分泌综合征。此类肿瘤大多为恶性肿瘤,其中以癌为多,如肺癌、胃癌、肝癌、胰腺癌、结肠癌等;也可见于肉瘤,如纤维肉瘤,平滑肌肉瘤、横纹肌肉瘤和未分化肉瘤等。许多分泌异位激素的恶性肿瘤都有产生两种以上激素的特点。关于异位激素产生的机制于今尚无一致的解释,可能与瘤细胞内基因异常表达有关。除上述异位内分泌综合征外,由于肿瘤的产物或异常免疫反应(包括交叉免疫、自身免疫和免疫复合物沉着等)或其他不明原因,还可引起神经、消化、造血、骨关节、肾及皮肤等系统发生一些病变和临床表现。这些表现不是由原发肿瘤或转移灶所在部位直接引起的,而是通过上述途径间接引起,故称为副肿瘤综合征(paraneoplastic syndrome)。有时这些综合征可以表现得非常明显而造成严重后果。认识此种综合征的意义在于它可能是一些隐匿肿瘤的早期表现,可由此而发现早期肿瘤。再者不要误认为这些系统的改变是由肿瘤转移所致,而放弃对肿瘤的治疗。与之相反,如肿瘤治疗有效,这些综合征可减轻或消失。因此有十分重要的临床意义。
良性肿瘤与恶性肿瘤的区别
综上所述,良性肿瘤和恶性肿瘤在生物学特点上是明显不同的,因而对机体的影响也不同。良性肿瘤一般对机体影响小,易于治疗,疗效好;恶性肿瘤危害较大,治疗措施复杂,疗效还不够理想。如果把恶性肿瘤误诊为良性肿瘤,就会延误治疗或治疗不彻底,造成复发、转移。相反,如把良性肿瘤误诊为恶性肿瘤,也必然要进行一些不必要、不恰当的治疗,使患者遭受不应有的痛苦、损害和精神负担。因此,区别良性肿瘤与恶性肿瘤,对于正确的诊断和治疗具有重要的实际意义。现将良性肿瘤与恶性肿瘤的区别列于表7-1。
表1 良性肿瘤与恶性肿瘤的区别
| 良性肿瘤 | 恶性肿瘤 | |
| 组织分化程度 | 分化好,异型性小,与原有组织的形态相似 | 分化不好,异型性大,与原有组织的形态差别大 |
| 核分裂 | 无或稀少,不见病理核分裂像 | 多见,并可见病理核分裂像 |
| 生长速度 | 缓慢 | 较快 |
| 生长方式 | 膨胀性和外生性生长,前者常有包膜形成,与周围组织一般分界清楚,故通常可推动 | 浸润性和外生性生长,前者无包膜,一般与周围组织分界不清楚,通常不能推动,后者每伴有浸润性生长 |
| 继发改变 | 很少性发生坏死、出血 | 常发生出血、坏死、溃疡形成等 |
| 转移 | 不转移 | 常有转移 |
| 复发 | 手术后很少复发 | 手术等治疗后较多复发 |
| 对机体影响 | 较小,主要为局部压迫或阻塞作用。如发生在重要器官也可引起严重后果 | 较大,除压迫、阻塞外,还可以破坏原发处和转移处的组织,引起坏死出血合并感染,甚至造成恶病质 |
必须指出,良性肿瘤与恶性肿瘤间有时并无绝对界限,有些肿瘤其表现可以介乎两者之间,称为交界性肿瘤(如卵巢交界性浆液性乳头状囊腺瘤和粘液性囊腺瘤)。此类肿瘤有恶变倾向,在一定的条件下可逐渐向恶性发展。在恶性肿瘤中,其恶性程度亦各不相同,有的较早发生转移,如鼻咽癌;有的转移晚,如子宫体腺癌;有的则很少发生转移。此外,肿瘤的良恶性也并非一成不变,有些良性肿瘤如不及时治疗,有时可转变为恶性肿瘤,称为恶性变(malignant change),如结肠腺瘤性息肉可恶变为腺癌。而个别的恶性肿瘤如黑色素瘤,有时由于机体免疫力加强等原因,可以停止生长甚至完全自然消退。又如见于少年儿童的神经母细胞瘤(neuroblastoma)的瘤细胞有时能发育成为成熟的神经细胞,有时甚至转移灶的瘤细胞也能继续分化成熟,使肿瘤停止生长而自愈。但这种情况毕竟罕见,绝大多数恶性肿瘤能否逆转为良性,是目前肿瘤研究的重要课题之一。
肿瘤的命名与分类
肿瘤的命名原则
人体任何部位、任何组织、任何器官几乎都可发生肿瘤,因此肿瘤的种类繁多,命名也复杂。一般根据其组织发生即组织来源来命名。良性肿瘤在其来源组织名称后加“瘤”字,例如来源于纤维结缔组织的良性瘤称为纤维瘤(fibroma),来源于腺上皮的良性瘤称为腺瘤(adenoma)等。有时还结合肿瘤的形态特点命名,如腺瘤呈乳头状生长并有囊腔形成者称为乳状头状囊腺瘤。恶性肿瘤一般亦根据其组织来源来命名。来源于上皮组织的统称为癌(carcinoma),命名时在其来源组织名称之后加“癌”字,如来源于鳞状上皮的恶性肿瘤称为鳞状细胞癌,来源于腺上皮呈腺样结构的恶性肿瘤称为腺癌等。从间叶组织(包括纤维结缔组织、脂肪、肌肉、脉管、骨、软骨组织等)发生的恶性肿瘤统称为肉瘤(sarcoma),其命名方式是在来源组织名称之后加“肉瘤”,例如纤维肉瘤、横纹肌肉瘤、骨肉瘤等。恶性肿瘤的外形具有一定的特点时,则又结合形态特点而命名,如形成乳头状及囊状结构的腺癌,则称为乳头状囊腺癌。如一个肿瘤中既有癌的结构又有肉瘤的结构,则称为癌肉瘤(carcinosarcoma)。
在病理学上,癌是指上皮组织来源的恶性肿瘤,但一般人所说的“癌症”(cancer),习惯上常泛指所有恶性肿瘤。
有少数恶性肿瘤不按上述原则命名,如有些来源于幼稚组织及神经组织的恶性肿瘤称为母细胞瘤,如神经母细胞瘤、髓母细胞瘤、肾母细胞瘤等;有些恶性肿瘤成分复杂或由于习惯沿袭,则在肿瘤的名称前加“恶性”,如恶性畸胞瘤、恶性淋巴瘤、恶性黑色素瘤等。有些恶性肿瘤冠以人名、如尤文(Ewing)瘤、何杰金(Hodgkin)病;或按肿瘤细胞的形态命名,如骨的巨细胞瘤、肺的燕表细胞癌。至于白血病、精原细胞癌则是少数采用习惯名称的恶性肿瘤,虽称为“瘤”或“病”,实际上都是恶性肿瘤。
肿瘤的分类
肿瘤的分类通常是以其组织发生(即来源于何种组织)为依据,每一类别又分为良性与恶性两大类。兹举例如下(表7-2)。
表7-2 肿瘤分类举例
| 组织来源 | 良性肿瘤 | 恶性肿瘤 | 好发部位 |
| 一、上皮组织 | |||
| 鳞状上皮 | 乳头状瘤 | 鳞状细胞癌 | 乳头状瘤见于皮肤、鼻、鼻窦、喉等处;鳞癌见于宫颈、皮肤、食管、鼻咽、肺、喉和阴茎等处 |
| 基底细胞 | 基底细胞癌 | 头面部皮肤 | |
| 腺上皮 | 腺瘤 | 腺瘤(各种类型) | 腺瘤多见于皮肤、甲状腺、胃、肠;腺癌见于胃、肠、乳腺、甲状腺等 |
| 粘液性或浆液性囊腺瘤 | 粘液性或浆液性囊腺癌 | 卵巢 | |
| 多形性腺瘤 | 恶性多形性腺瘤 | 涎腺 | |
| 移行上皮 | 乳头状瘤 | 移行上皮癌 | 膀胱、肾盂 |
| 二、间叶组织 | |||
| 纤维结缔组织 | 纤维瘤 | 纤维肉瘤 | 四肢 |
| 纤维组织细胞 | 纤维组织细胞瘤 | 恶性纤维组织细胞瘤 | 四肢 |
| 脂肪组织 | 脂肪瘤 | 脂肪肉瘤 | 前者多见于皮下组织,后者多见于下肢和腹膜后 |
| 平滑组织 | 平滑肌瘤 | 平滑肌肉瘤 | 子宫和胃肠 |
| 横纹肌组织 | 横纹肌瘤 | 横纹肌肉瘤 | 肉瘤多见于头颈、生殖泌尿道及四肢 |
| 血管和淋巴管组织 | 血管瘤、淋巴管瘤 | 血管肉瘤 淋巴管肉瘤 | 皮肤和皮下组织、舌、唇等 |
| 骨组织 | 骨瘤 | 骨肉瘤 | 骨瘤多见于颅骨、长骨;骨肉瘤多见于长骨两端,以膝关节上下尤为多见 |
| 巨细胞瘤 | 恶性巨细胞瘤 | 股骨上下端、胫骨上端、肱骨上端 | |
| 软骨组织 | 软骨瘤 | 软骨肉瘤 | 软骨瘤多见于手足短骨;软骨肉瘤多见于盆骨、肋骨、股骨、肱骨及肩胛骨等 |
| 滑膜组织 | 滑膜瘤 | 滑膜肉瘤 | 膝、踝、肩和肘等关节附近 |
| 间皮 | 间皮瘤 | 恶性间皮瘤 | 胸膜、腹膜 |
| 三、淋巴造血组织 | |||
| 淋巴组织 | 恶性淋巴瘤 | 颈部、纵隔、肠系膜和腹膜后淋巴结 | |
| 造血组织 | 各种白血病 | 淋巴造血组织 | |
| 多发性骨髓瘤 | 椎骨、胸骨、肋骨、颅骨和长骨 | ||
| 四、神经组织 | |||
| 神经衣组织 | 神经纤维瘤 | 神经纤维肉瘤 | 单发性;全身皮神经;多发性:深部神经及内脏也受累 |
| 神经鞘细胞 | 神经鞘瘤 | 恶性神经鞘瘤 | 头、颈、四肢等处神经 |
| 胶质细胞 | 胶质细胞瘤 | 恶性胶质细胞瘤 | 大脑 |
| 原始神经细胞 | 髓母细胞瘤 | 小脑 | |
| 脑膜组织 | 脑膜瘤 | 恶性脑膜瘤 | 脑膜 |
| 交感神经节 | 节细胞神经瘤 | 神经母细胞瘤 | 前者多见于纵隔和腹膜后,后者多见于肾上腺髓质 |
| 五、基他肿瘤 | |||
| 黑色素细胞 | 黑痣 | 恶性黑色素瘤 | 皮肤、粘膜 |
| 胎盘组织 | 葡萄胎 | 绒毛膜上皮癌、恶性葡萄胎 | 子宫 |
| 性索 | 支持细胞、间质细胞瘤 | 恶性支持细胞、间质细胞瘤 | 卵巢、睾丸 |
| 颗粒细胞瘤 | 恶性颗粒细胞瘤 | 卵巢 | |
| 生殖细胞 | 精原细胞瘤 | 睾丸 | |
| 无性细胞瘤 | 卵巢 | ||
| 胚胎性癌 | 睾丸、卵巢 | ||
| 三个胚叶组织 | 畸胎瘤 | 恶性畸胎瘤 | 卵巢、睾丸、纵隔和骶尾部 |