三氯化碘为可燃酸性腐蚀品。
历史
是较早发现的互卤化物之一,早在1814年即与一氯化碘一起被戴维发现。
IUPAC名
iodine trichloride
CAS
865-44-1
PubChem
70076
化学式
ICl3 (单体);
I2Cl6 (二聚体)
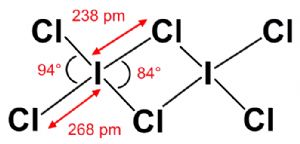
三氯化碘的二聚体结构
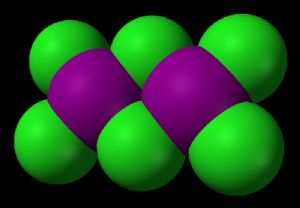
三氯化碘二聚体的空间填充模型
摩尔质量
(二聚体) 466.5281 g·mol?1
密度
3.117 g/cm3 (15℃)
熔点
33℃
沸点
77℃ (分解)
分解温度
25℃
欧盟危险性符号
 腐蚀性 C
腐蚀性 C
警示术语
R:R34, R37
安全术语
S:S26, S36/37/39, S45
性质
黄棕色针状易潮解结晶,在室温下能挥发。有刺鼻气味。具腐蚀性。熔点 33℃。加热至 77℃完全分解为一氯化碘和氯气。溶于水分解,溶于乙醇、苯、乙醚、四氯化碳和浓盐酸等。一般配成20~35%的浓盐酸溶液使用。由于易分解,因此很难得到纯的产品。
固态时三氯化碘的晶体是一个平面分子结构,属三斜晶系,其简单晶格不是以 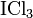 存在而是
存在而是 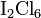 。
。
熔融的三氯化碘会明显地发生离解,生成一氯化碘和氯气:

因此作为溶剂是不适宜的。另一方面 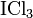 的电导测定又表明有以下反应发生:
的电导测定又表明有以下反应发生:
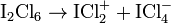
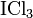 也可以与路易斯酸生成
也可以与路易斯酸生成 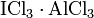 之类的配合物。
之类的配合物。
与水反应生成一氯化碘、盐酸和碘酸:
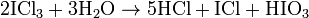
制备
1、由碘和定量的液氯在 ?80℃反应制备。蒸发除去过剩氯后获得固态六氯化二碘,不能用结晶法或蒸馏法纯化,因为它迅速分解为一氯化碘和氯气。
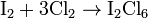
2、在<40℃的强酸性溶液中进行如下反应。
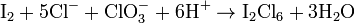
此法是制备六氯化二碘的方便方法。
用途
用于医药、有机合成和测定碘值。用作氯化剂及氧化剂。