2 英文参考
Evaluation requirement of indicators for medical purpose-low temperature steam and formaldehyde sterilization processes
3 基本信息
ICS 11.080
C 59
中华人民共和国卫生行业标准WS/T 651—2019《医用低温蒸汽甲醛灭菌指示物评价要求》(Evaluation requirement of indicators for medical purpose-low temperature steam and formaldehyde sterilization processes)由中华人民共和国国家卫生健康委员会于2019年01月30日《关于发布〈过碳酸钠消毒剂卫生要求〉等6项推荐性卫生行业标准的通告》(国卫通〔2019〕4号)发布,自2019年07月01日起实施。
4 发布通知
关于发布《过碳酸钠消毒剂卫生要求》等6项推荐性卫生行业标准的通告
国卫通〔2019〕4号
现发布《过碳酸钠消毒剂卫生要求》等6项推荐性卫生行业标准,编号和名称如下:
WS/T 647—2019 溶葡萄球菌酶和溶菌酶消毒剂卫生要求
WS/T 651—2019 医用低温蒸汽甲醛灭菌指示物评价要求
上述标准自2019年7月1日起施行。
特此通告。
国家卫生健康委员会
2019年1月30日
5 前言
本标准按照 GB/T1.1—2009 给出的规则起草。
本标准起草单位:山东省疾病预防控制中心、中国疾病预防控制中心环境与健康相关产品安全所、江苏省疾病预防控制中心、山东省精神卫生中心、广东检验检疫技术中心、临沭县安全生产监督管理局、潍坊医学院。
本标准主要起草人:崔树玉、杨彬、张流波、李子尧、刘雷、苏冠民、孙文魁、张剑、沈瑾、孙惠惠、陈璐、董非、孟蔚、赵克义、温宪芹、徐燕、孙启华、廖如燕、田忠梅、刘晓康、周建芳、邹以华、杨静、谢卡罗、王晓云。
6 标准正文
6.1 1 范围
本标准规定了医用低温蒸汽甲醛灭菌指示物的分类、通用要求、化学指示物要求及生物指示物要求。
本标准适用于通过化学、生物指标的变化反映医用低温蒸汽甲醛灭菌过程的指示物。
6.2 2 规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅所注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB 18281.1 医疗保健产品灭菌 生物指示物 第1部分:通则
消毒产品标签介绍管理规范(2005年) 卫生部(卫监督发〔2005〕426号)
6.3 3 术语和定义
下列术语和定义适用于本文件。
3.1
低温蒸汽甲醛灭菌 low temperature steam and formaldehyde sterilization
在温度低于85℃时,强制排出空气后,负压状态下注入蒸汽甲醛,待灭菌物品暴露于蒸汽甲醛,在稳定的状态下维持一定时间,达到灭菌要求。
3.2
化学指示物 chemical indicator
指示剂及其载体按预定形式的组合,暴露于低温蒸汽甲醛灭菌程序中一个或多个预定过程变量而产生化学或物理变化。
3.3
生物指示物 biological indicator
3.4
D值 D value
3.5
3.6
6.4 4 指示物分类
6.4.1 4.1 化学指示物
6.4.1.1 4.1.1 灭菌过程指示物
指示每个独立单元的灭菌物品是否经过灭菌程序,包括卡、胶带、标签等。
6.4.1.2 4.1.2 灭菌效果指示物
用于证明独立单元物品经过整个灭菌程序后,是否达到所选参数的设定值。
6.4.2 4.2 生物指示物
4.2.1 按结构可分为片状生物指示物和自含式生物指示物,片状生物指示物需要使用阳性对照和阴性对照,而自含式生物指示物只需要阳性对照即可。
4.2.2 按培养时间可分为常规型生物指示物和快速型生物指示物。
6.5 5 指示物通用要求
5.1 医用低温蒸汽甲醛灭菌过程评价参数应包括作用时间、温度、甲醛浓度。
5.2 包装标签和介绍应符合《消毒产品标签介绍管理规范》的要求。
5.3 指示物应标明其用途。
5.4 指示物应根据使用用途与不同的过程挑战装置相组合,模拟灭菌因子最难达到的部位。
5.5 指示物应标明储存条件和效期。
5.6 经符合各项预设参数的灭菌周期后,指示物变化应与生产商规定的合格要求一致;若预设的最低限度参数不符合或预设的参数不合理,则指示物变化应与生产商规定的合格要求不一致。
5.7 用于日常监测的生物指示物应与化学指示物同时使用,二者均合格,才能视为达到灭菌效果。
5.8 指示物包装材料和载体应避免选择对甲醛有吸附作用的材质,且应不影响指示物的使用,确保其无害。
5.9 取包装完好的指示物放置于生产商标明储存条件下,存放至规定的效期,取出再次进行评价,指示物应满足本标准规定的技术要求。
6.6 6 化学指示物要求
6.6.1 6.1 灭菌过程化学指示物
灭菌过程化学指示物应按表1设定的条件进行测试并符合要求。测定方法见附录A。
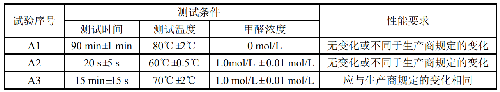
注1:若过程化学指示物仅标明在低于 55℃或高于 65℃的温度下灭菌周期使用,则表 1 中的测试应在生产商规定的最高温度和甲醛浓度下进行。
注2:为了证明对特殊过程的适用性,应增加生产商规定的低温蒸汽甲醛灭菌程序进行附加的功能测试。
6.6.2 6.2 灭菌效果化学指示物
灭菌效果化学指示物应按表2设定的条件进行测试并符合要求。测定方法见附录A。
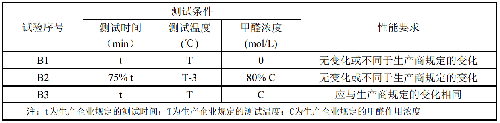
注:t为生产企业规定的测试时间;T为生产企业规定的测试温度;C为生产企业规定的甲醛作用浓度
6.7 7 生物指示物要求
6.7.1 7.1 指示菌
7.1.1 指示菌株应为嗜热脂肪地芽胞杆菌或者是相当性能的其他菌株。推荐嗜热脂肪地芽胞杆菌有NCIB 8224、 DSM 6790、 ATCC 7953、 ATCC 10149 和 ATCC 12980 用于试验,制备成芽胞。如果使用其他的菌株,应首先测定其抗力。
7.1.2 由生产企业提供的最终产品应无杂菌。
6.7.2 7.2 指示菌数量和抗力
7.2.1 生产企业应标明指示菌的数量和抗力特性。
7.2.2 指示菌活菌数应≥1.0×105CFU/载体。对于成品的指示物,载体回收的菌量与介绍上的菌量误差在–50%~+300%之间。测定方法见附录 B。
7.2.3 在 60℃条件下,以时间(min)为单位的 D 值表示指示菌的抗力,精确到小数点后一位。每批次/批号的生物指示物或染菌载体都应标注相应的 D 值。
7.2.4 生物指示物中指示微生物的 D 值应≥6.0 min;其它指示微生物应当具有符合使用条件的 D 值。
测定方法见附录 C。
7.2.5 D 值的验证,按附录 C 测定方法。ST 值验证 D 值,样本应全部有菌生长;KT 值验证 D 值,样本应全部无菌生长。ST 值和 KT 值分别按式(1)和式(2)计算。

式中:
ST——存活时间,单位为分钟(min);
KT——杀灭时间,单位为分钟(min);
N0——每批生物指示物的回收菌量的平均数,单位为CFU/载体。
6.7.3 7.3 载体和内层包装
7.3.1 测试应满足下列条件:
a) 暴露温度:同生产商规定载体和内层包装的最高暴露温度;如果生产商没有规定,暴露温度至少为 100℃。
b) 暴露时间:至少为 160 min。
7.3.2 在灭菌处理中及灭菌后,生物指示物系统的任何材料,不应残留或释放出任何抑制试验菌生长的物质。测定方法按照 GB 18281.1 进行。
7 附录A(规范性附录)化学指示物检测方法
7.1 A.1 检测仪检测法
A.1.1 检测仪应能设置、监测与确认温度、时间、甲醛浓度等参数。
A.1.2 灭菌过程化学指示物置于检测仪内,按表1要求的测试条件进行测试;灭菌效果化学指示物置于检测仪内,按表2要求的测试条件进行测试。
A.1.3 同批次化学指示物每次试验测试不少于10个,试验不少于3次。
7.2 A.2 甲醛溶液检测法(仅适用于不具有吸水性能的材质制备的化学指示物检测)
A.2.1 灭菌过程指示物根据6.1的要求配制甲醛水溶液,灭菌效果指示物根据6.2的要求配制甲醛水溶液。
A.2.3 将化学指示物置于固定的样品架上,样品架不应影响化学指示物的性能。
A.2.4 将样品架置于预热的甲醛溶液中,确保化学指示物浸泡在甲醛溶液里,按6.1或6.2规定时间测试。
A.2.5 从甲醛溶液中取出样品架,去除多余的甲醛,1.5 min内指示物呈现的颜色维持在一定水平不再变化,检测指示物的性能,记录结果。
8 附录B(规范性附录)生物指示物活菌数测定
B.2 取含有 10mLTPS(0.1%胰蛋白胨的生理盐水溶液)的无菌试管,加入适量无菌玻璃珠,将生物指示物染菌载体投入试管,用电动混合器充分混合,制成菌悬液。
B.3 选择适宜稀释度菌悬液,吸取其中混合均匀的悬液 1.0mL 加于无菌平皿内。每一稀释度接种 2个平皿。一般需接种 2 个~3 个稀释度。
B.4 将 40℃~45℃ 熔化的嗜热脂肪杆菌芽胞恢复培养基或相应的培养基倾注于已加入菌悬液的平皿中,每平皿 15mL~20mL。
B.5 待琼脂凝固后,翻转平板使底向上,置 56℃±2℃恒温培养箱内培养。
B.6 培养至 72h,计数菌落数。一般以肉眼观察,必要时用放大镜检查。报告菌落数在 15CFU~300CFU 的稀释度的结果。
9 附录C(规范性附录)微生物抗力测定方法
9.1 C.1 接种载体暴露条件
C.1.1 水溶液中甲醛浓度1mol/L±0.01mol/L。
C.1.2 暴露温度60℃±0.5℃。
C.1.3 暴露时间能维持在1min~150min,精确度在±10s。
9.2 C.2 方法
C.2.1 取10mL甲醛溶液置于试管中,预先加热至暴露温度,将生物指示物载体完全浸入其中。
C.2.2 确保载体完全浸泡在甲醛溶液中,并尽量减少试管振动。
C.2.3 严格执行无菌操作。
C.2.5 去除载体表面多余的液体后,将其置于含2%的亚硫酸钠溶液中和剂中至少10min,用以中和残留的甲醛溶液。密封试管,并尽量减少振动,以防止载体上的受试微生物脱落。
注:2%的亚硫酸钠溶液可用过滤除菌的方式进行处理。也可使用其它验证有效的中和剂。
C.2.6 选择适合的培养基复苏受试微生物。建议选择大豆酪蛋白消化培养基。
C.2.8 将试管置于90℃,60min。
C.2.9 活菌数测定,参见附录B。
9.3 C.3 用微生物存活曲线法测定 D 值
C.3.2 至少有 5 次暴露,包括
b) 有 1 次暴露使活菌总数至少减少到初始接种量的 0.01%,且存活菌量大于 50CFU;
C.3.3 每 2 次相邻暴露的时间间隔应相等。
C.3.4 每次测定中每次暴露所用的染菌载体应不少于4个,每次暴露必须采用数目相同的同样的试样。
C.3.5 每次暴露后,按 C.2.4~C.2.9 对试样进行处理。
C.3.6 用所得的全部存活菌数的常用对数值,对时间 (min) 作图,用最小二乘法进行回归分析,确定最佳线性曲线。回归分析时不应包括原先接种细菌数 0.51og 范围内的存活数据点。计算所得直线斜率的负倒数值,即等于以分钟表示的D值,数据举例见表C.1。
C.3.6.1 最佳线性曲线斜率按式(C.1)计算:

式中:
m ——最佳线性曲线斜率;
n ——数据点之和;
A ——暴露间隔时间之和;
B ——存活菌数的对数值之和;
C ——暴露间隔时间平方之和。

注:回归分析时不应包括0.5 log10y1范围内的存活数据点
C.3.6.2 D值按式(C.2)计算:
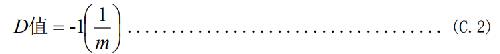
C.3.7 所得存活菌曲线的线性相关系数应不小于0.8。线性相关系数按式(C.3)计算:
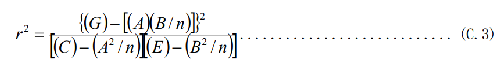
式中:
E ——存活菌数的对数值平方之和。
9.4 C.4 用部分阴性分析法计算D值
C.4.2 至少有5种暴露,包括:
C.4.3 每2次相邻暴露的时间间隔应相等。
C.4.4 每次测定中每次暴露所用的染菌载体应不少于20个,每次暴露应采用相同数目同样的试样。
C.4.5 每次暴露后,试样接种含中和剂的增菌液,按生产厂商规定的温度和时间进行培养后观察结果,数据示例见表C.2。
C.4.6 D值的计算
C.4.6.1 有限Holcomb-Spearman-Karber法(LHSKP),灭菌的平均时间按式(C.4)计算:
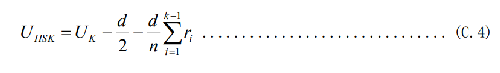
式中:
d —— 暴露的时间间隔,各间隔完全相同;
n —— 每次暴露的测试样本量,要求每次暴露的样本量相同,如均为20个;
N0 —— 通过总活菌计数法(见附录B)获得的每个指示剂活菌计数的平均值;

C.4.6.3 方差按式(C.6)计算:

C.4.6.4 标准差按式(C.7)计算:

C.4.6.5 D 值95%的可信区间(p=0.05)Dcalc按式(C.8)计算:
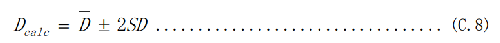
C.4.6.6 D值可信区间上限按式(C.9)计算:

C.4.6.7 D值可信区间下限按式(C.10)计算:

表C.2 LHSKP 测定 D 值数据示例

注:如果经过U1暴露(如没有阴性样本,r=0),且经过相继暴露的UK所有重复试验均为阴性(r= n)(如都不生长),则测试为有效。
9.5 C.5 D 值的验证
C.5.1 ST 值验证 D 值
将50个试验样本放入C.1 规定的暴露条件下,暴露时间设定为计算出的ST值,暴露完成后,将样本取出接种含中和剂的增菌液,按生产商规定的温度和时间进行培养后观察结果。
C.5.2 KT 值验证 D 值
将50个试验样本放入C.1规定的暴露条件下,暴露时间设定为计算出的KT值,暴露完成后,将样本取出接种含中和剂的增菌液,按生产商规定的温度和时间进行培养后观察结果。